Genetische Kardiomyopathie-Marker – Kombination der Bildgebung mit Labordiagnostik
Beschwerden, die das Herz betreffen, können auf verschiedenen Ursachen beruhen und zu unterschiedlichen kardialen Pathologien, wie der koronaren Herzkrankheit (KHK, Erkrankung der Herzkranzgefäße), Bluthochdruck (Hypertonie) oder Herzklappenerkrankungen führen. Aber auch angeborene Herzfehler kommen als Auslöser der Symptome infrage.
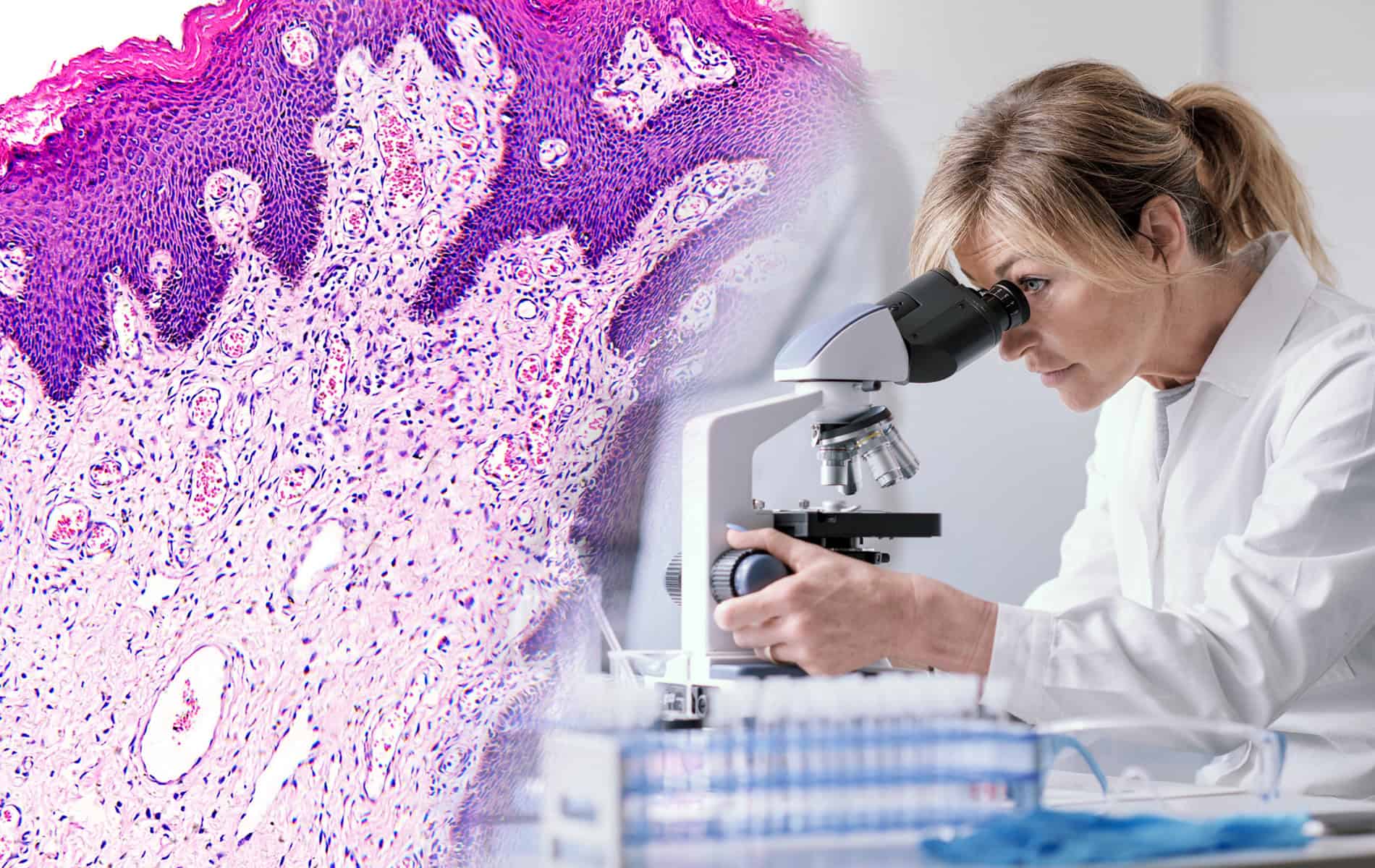
Lassen sich keine der genannten Krankheitsbilder identifizieren bei gleichzeitig vorliegender funktioneller und struktureller Einschränkung des Herzmuskels, geht der Verdacht oft in Richtung Kardiomyopathie. Aufgrund der Unterschiede im Erscheinungsbild, das von Patient zu Patient variieren kann, ist die Diagnosestellung oft komplex. Die Labordiagnostik – insbesondere die Bestimmung genetischer Marker – spielt zur Abgrenzung verschiedener Varianten der Kardiomyopathie eine Rolle, da die familiäre Häufung dieser Typen auf eine genetische Komponente hinweist.
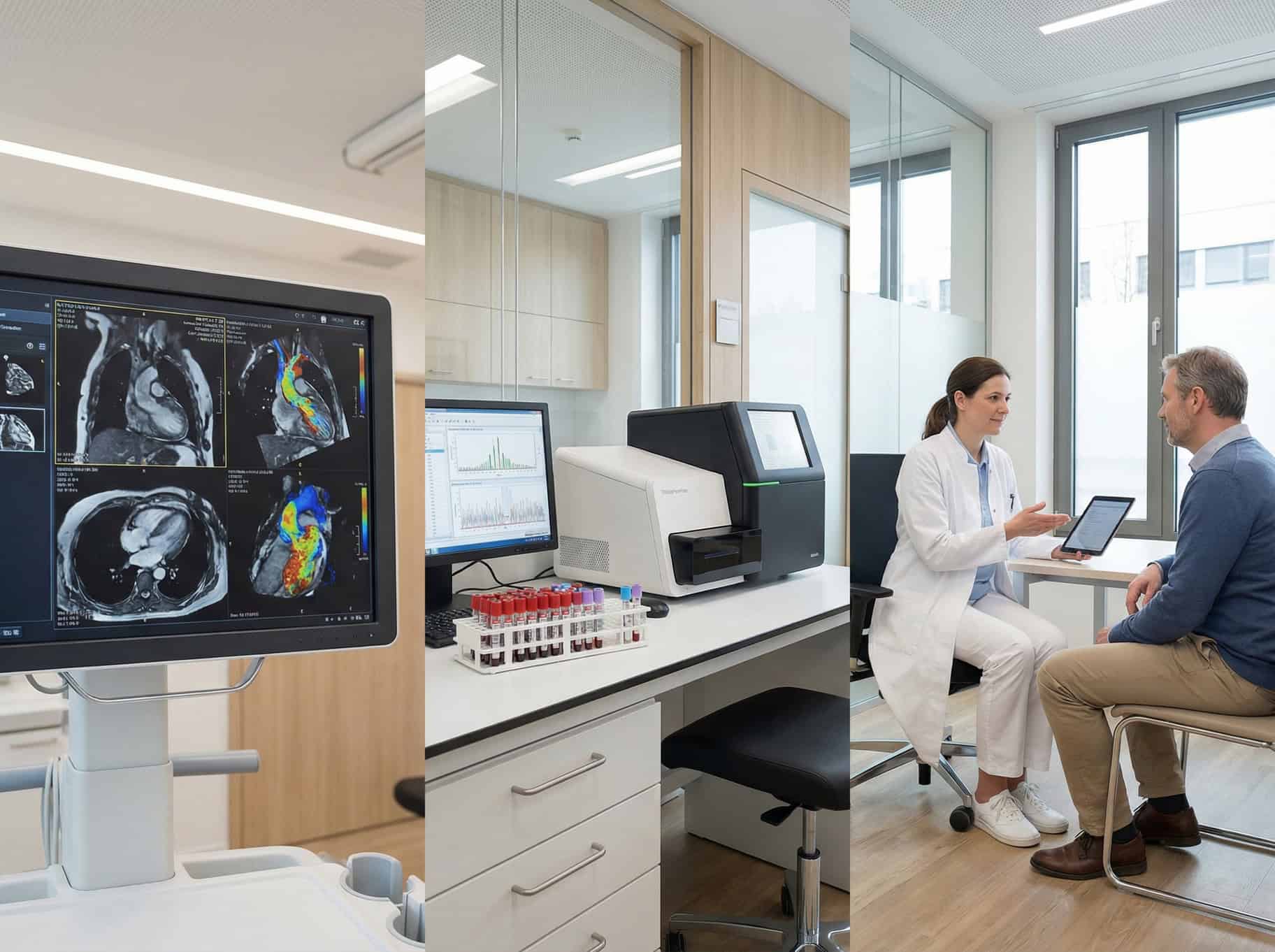
Formen und Symptome der Kardiomyopathie
Wichtige Fakten auf einen Blick:
- Kardiomyopathien zeigen sich durch oft eher unspezifische Symptome.
- Auslöser können auch genetische Faktoren sein, was eine familiäre Häufung bestimmter Befunde nahelegt.
- Diagnostisch greifen Anamnese, Labor mit Genetik und Bildgebung ineinander.
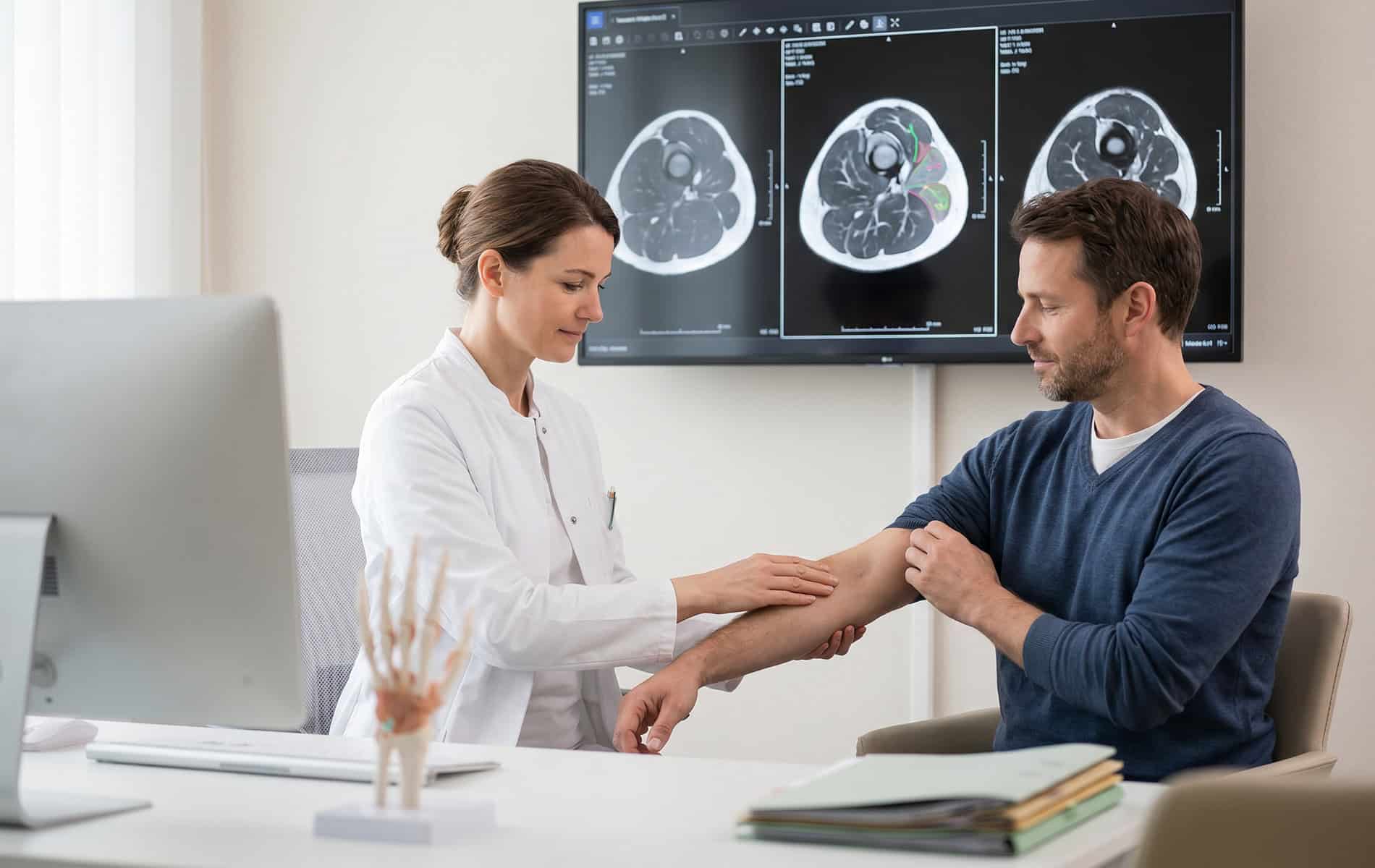
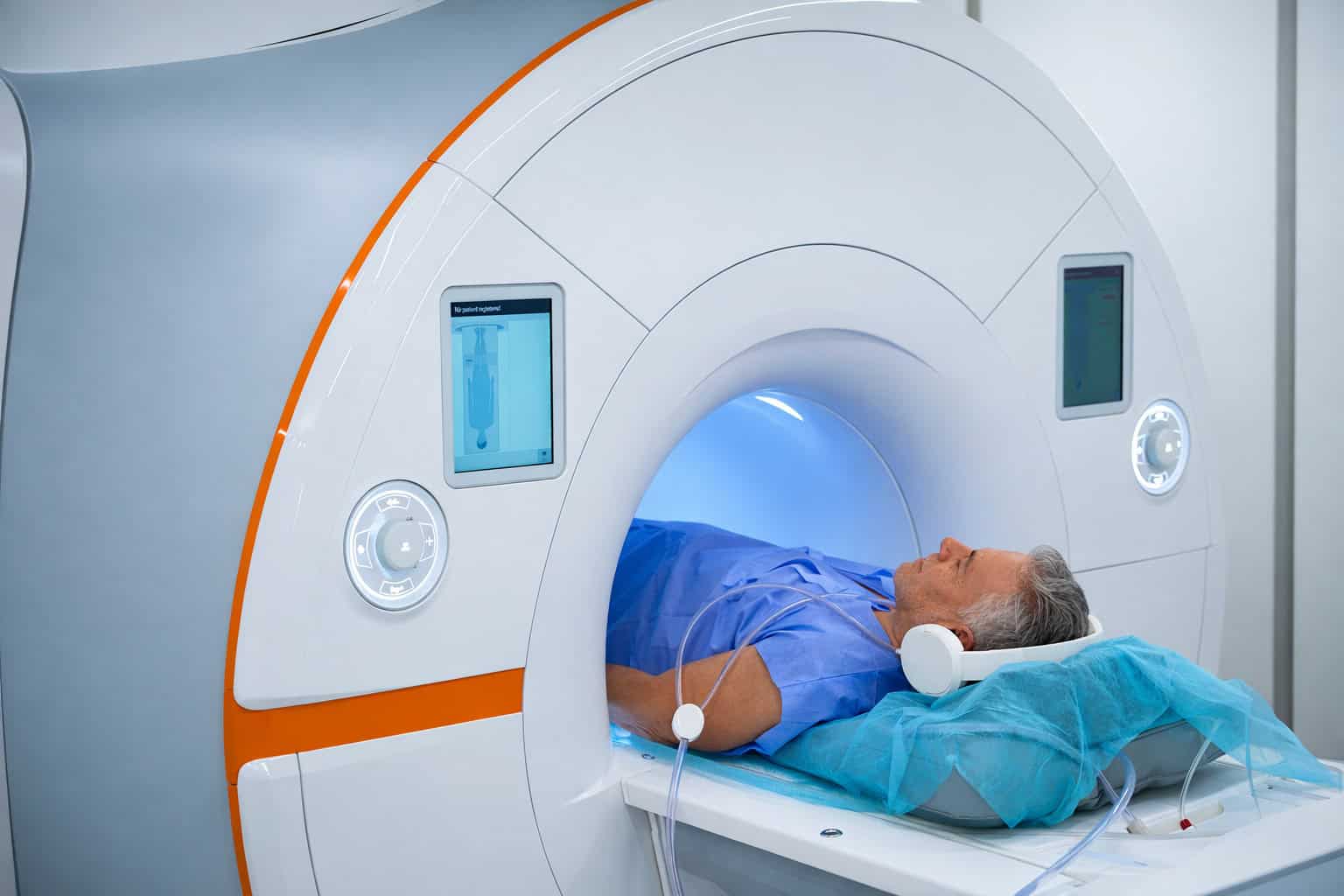
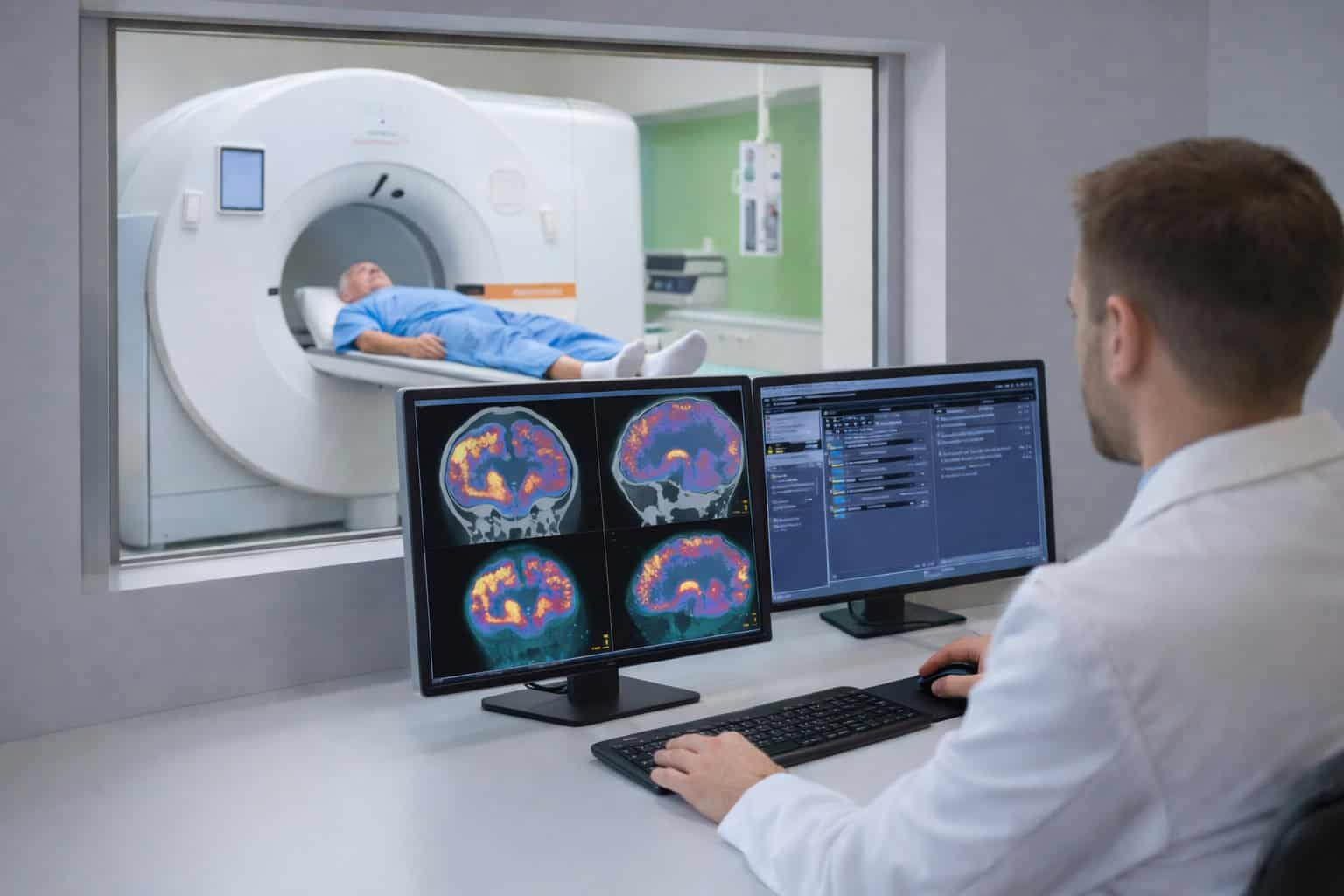
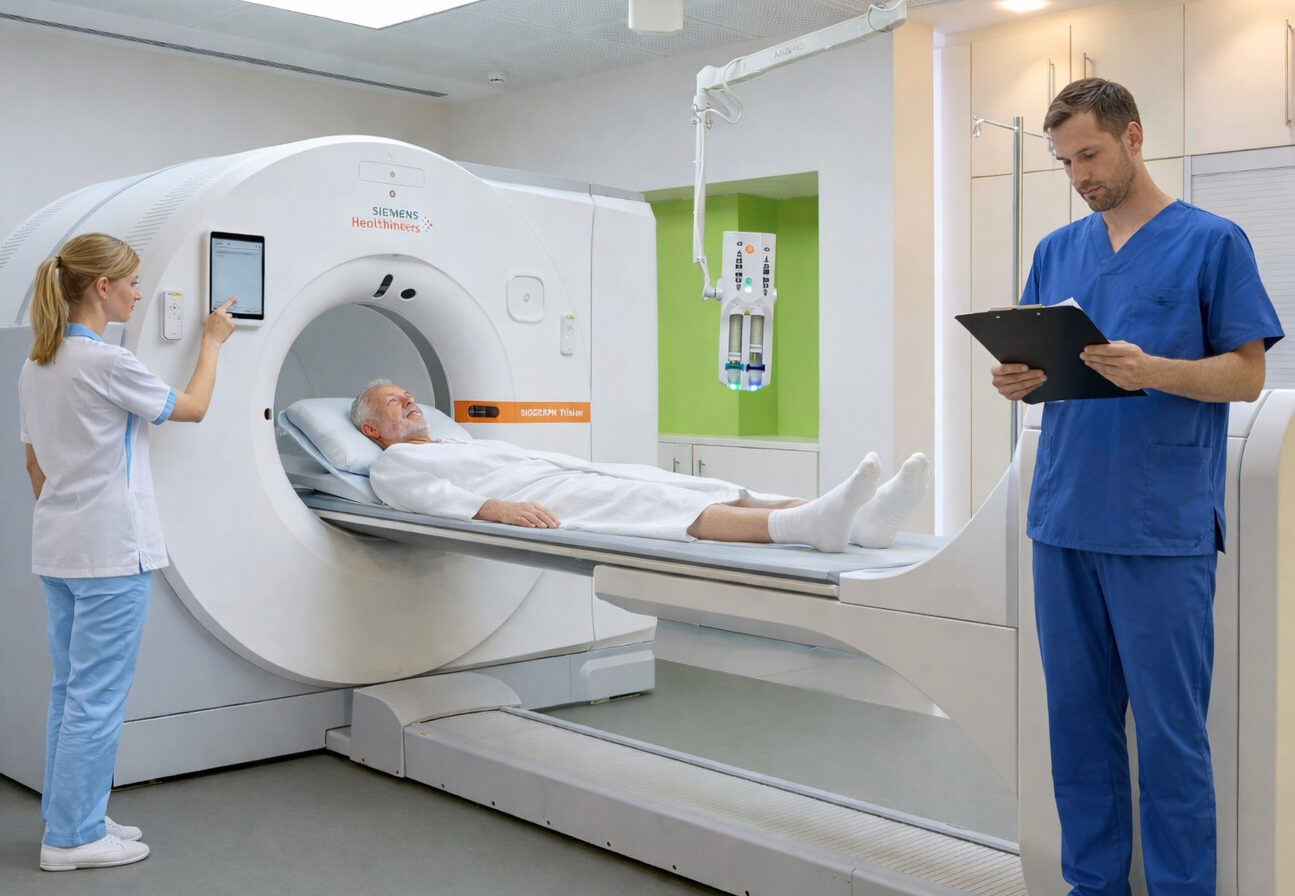
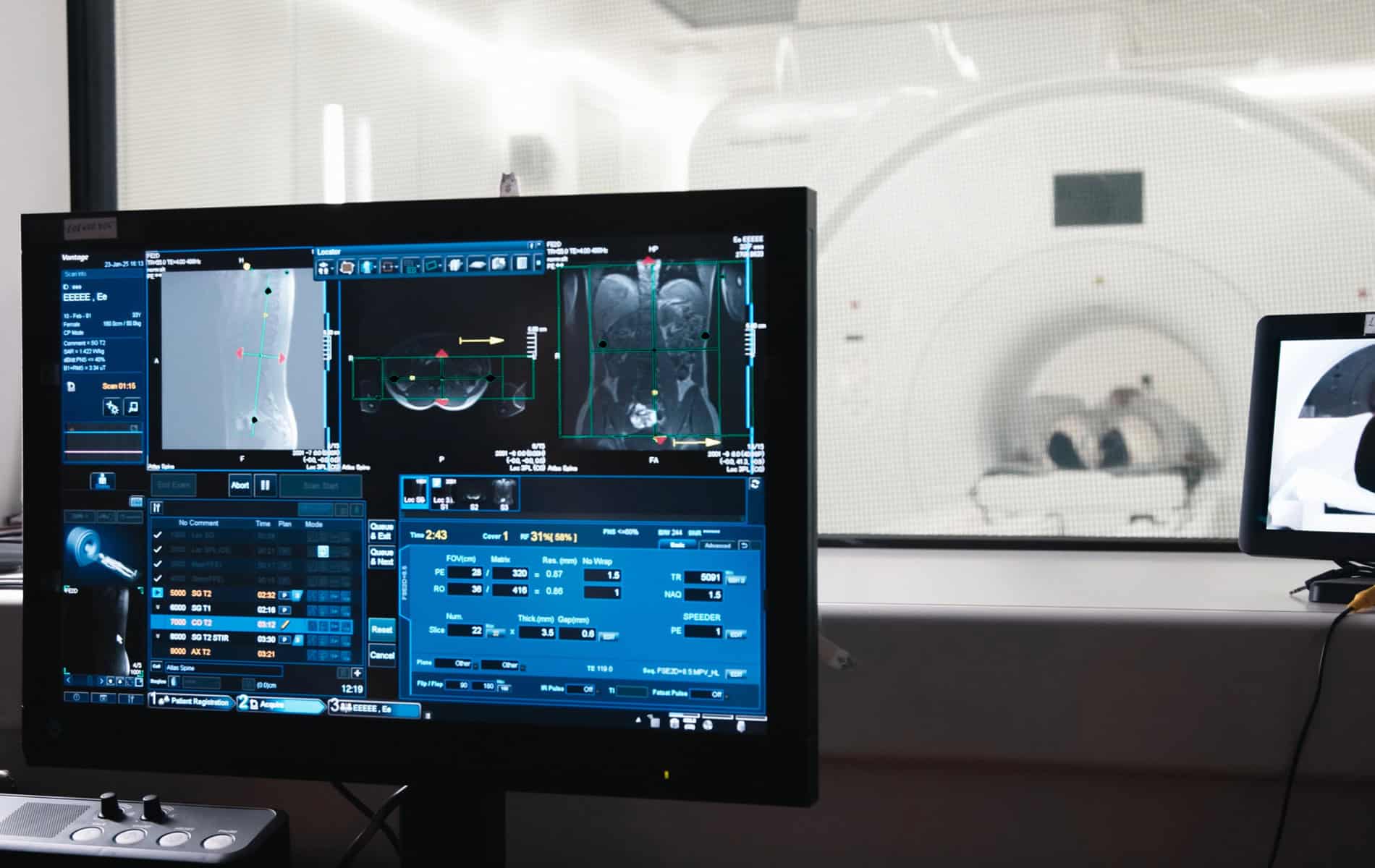
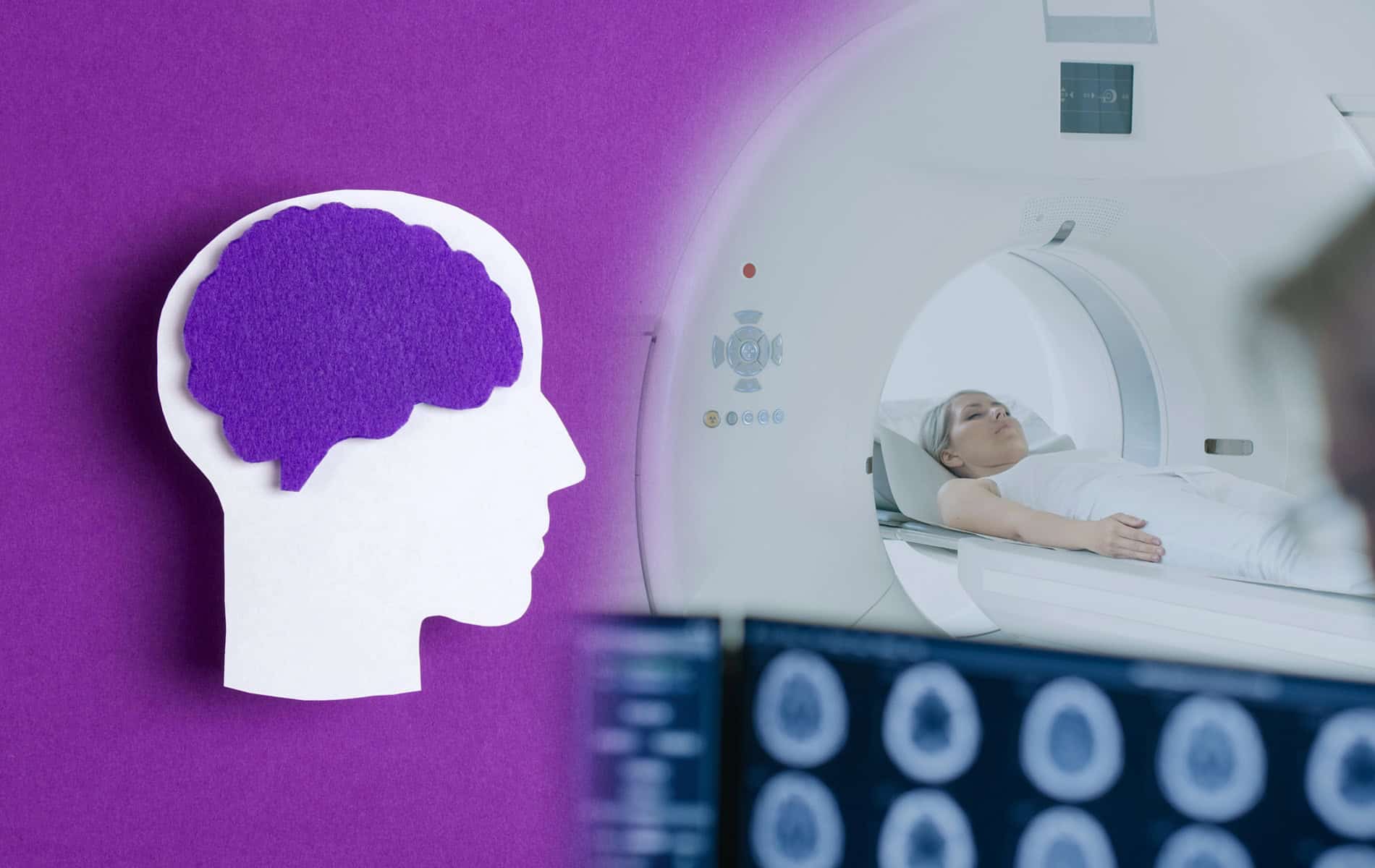
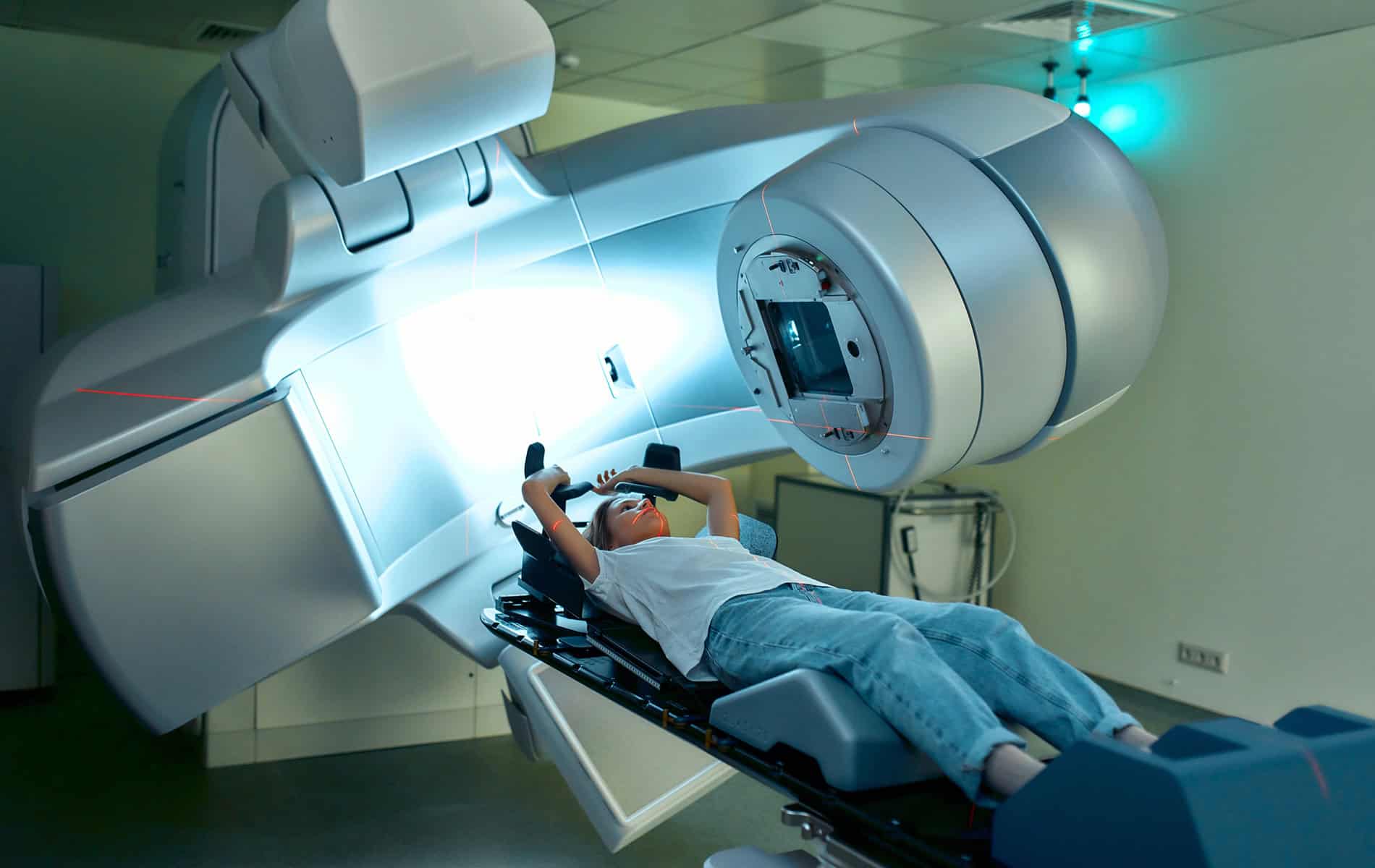
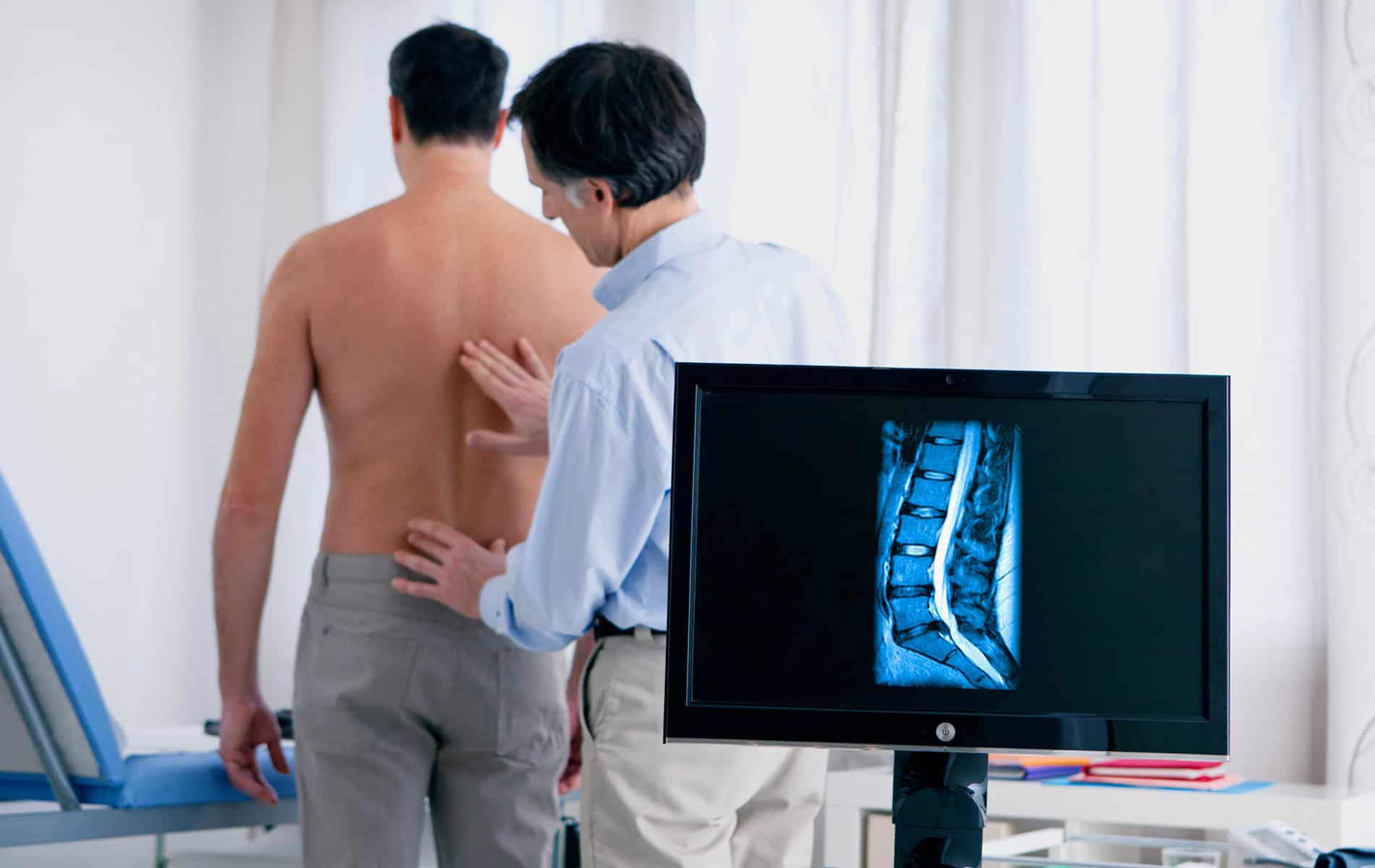
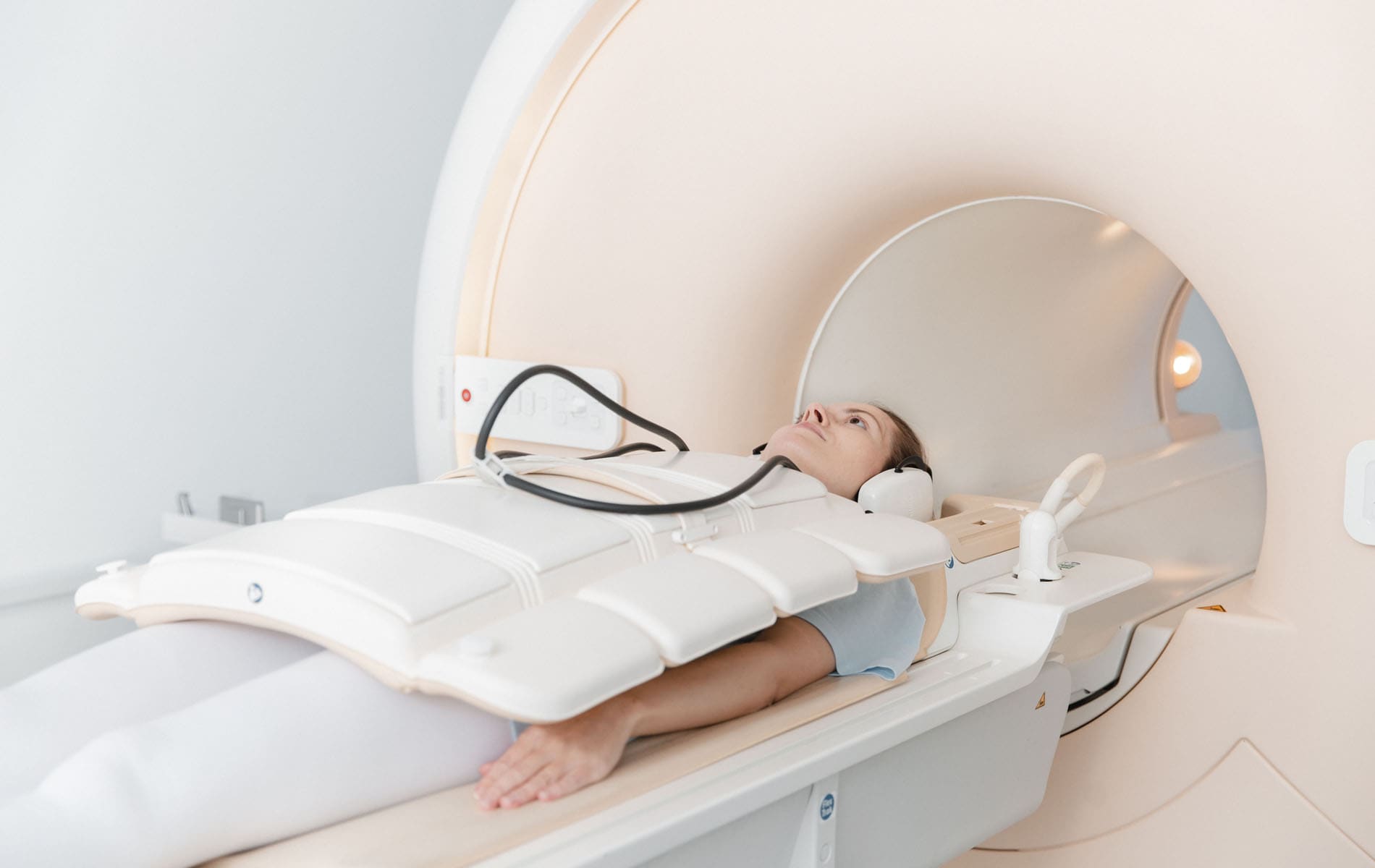
Kardiomyopathien lassen sich anhand unterschiedlicher Kriterien einteilen, wobei der Phänotyp-basierte Ansatz meist im Vordergrund steht. Dieser fußt auf dem Erscheinungsbild, das sich klinisch in den Funktionsuntersuchungen und der Bildgebung (zum Beispiel mittels Kardio-MRT) zeigt.
- Die hypertrophe Kardiomyopathie (HCM) ist durch eine Verdickung der Herzmuskelwand gekennzeichnet, ohne dass eine Druckbelastung (zum Beispiel durch Bluthochdruck) dafür als Ursache identifiziert werden kann.
- Die nicht dilatative linksventrikuläre Kardiomyopathie (NDLVC) ist durch das Vorhandensein von nicht auf Durchblutungsstörungen zurückzuführende Narben oder Fetteinlagerungen in der linken Herzkammer (Ventrikel) gekennzeichnet (Beschwerden entstehen unabhängig von globalen oder regionalen Wandbewegungsstörungen). Die Bewegungsstörung kann aber auch ohne Narbenbildung (betrifft die linke Herzkammer global) entstehen.
- Eine dilatative Kardiomyopathie (DCM) zeigt sich durch eine Erweiterung und Funktionsschwäche der linken oder beider Herzkammern. Sie ist eine häufige Ursache einer Herzinsuffizienz (Herzschwäche) bei jüngeren Menschen.
- Die arrhythmogene Kardiomyopathie (ACM) betrifft vorwiegend die rechte Herzkammer und geht mit einem erhöhten Risiko für gefährliche Herzrhythmusstörungen einher. Bei der ACM treten viele Fälle (bis 50 Prozent) mit einer familiären Häufung auf [1].
- Die restriktive Kardiomyopathie (RCM) ist eine Dysfunktion, die eine oder beide Herzkammern betreffen kann und mit einem normalen oder reduzierten diastolischen und systolischen Volumen (die Diastole ist die Füllungsphase, die Systole die Auswurfphase) sowie einer normalen Wanddicke der Herzkammern einhergeht.
Zu den Herausforderungen in der Diagnostik gehört das häufig unspezifische klinische Bild.
Die typischen Beschwerden wie Atemnot bei körperlicher Anstrengung (Belastungsdyspnoe) oder Herzrasen oder -stolpern (Palpitationen) können auch mit verschiedenen anderen kardiologischen Pathologien in Zusammenhang stehen.
Genetische Marker bei Kardiomyopathie: Welche Gene sind relevant?
Wichtige Fakten auf einen Blick:
- Die Medizin hat in den letzten Jahren verschiedene Genmutationen im Zusammenhang mit Kardiomyopathien entdeckt.
- Für einige der Genvarianten wird von einer höheren Pathogenität ausgegangen und somit in der Regel eine schlechtere Prognose gestellt.
- Nach der Analyse (Gensequenzierung) werden die gefundenen Genvarianten klassifiziert.
Vor dem Hintergrund, dass die Medizin von den molekularbiologischen Forschungen der zurückliegenden Jahre in verschiedenen Bereichen profitiert hat und für diverse Krankheitsbilder immer wieder kritische Gensequenzen entdeckt werden, erklärt sich auch die zunehmende Bedeutung genetischer Marker für die Diagnostik von Kardiomyopathien.
Die Forschung hat für die verschiedenen Varianten der Erkrankung unterschiedliche Gene identifiziert, die sich pathologisch auffällig verhalten.
- Hypertrophe Kardiomyopathie (HCM): Hier treten unter anderem Mutationen in Sarkomer-Genen (kodieren bestimmte Eiweiße des kontraktilen Apparats der Herzmuskelzelle) auf. In einer Studie wurden bei mehr als einem Drittel der auf HCM getesteten Patienten pathogene Genotypen identifiziert [2]. Darüber hinaus hat die Medizin inzwischen weitere Gene, unter anderem jene, die mit dem wichtigen Herzinfarktmarker Troponin in Zusammenhang stehen (TNNI3, TNNT2), identifiziert. Das Konsenspapier der Deutschen Gesellschaft für Kardiologie führt außerdem noch weitere Gene, wie Transthyretin (TTR, relevant für die Amyloid-Kardiomyopathie als Differenzialdiagnose) oder PRKAG2 auf [3].
- Dilatative Kardiomyopathie (DCM): Diese Form verfügt ebenfalls über ein sehr breites Spektrum verschiedener Gene, die von Mutationen betroffen sein können, wozu LMNA (kodiert Strukturproteine der inneren Zellkernmembran), MYBPC3 (kodiert ein Strukturprotein im Herzmuskel), SCN5A (für den Natriumkanal und Zelltransporte zuständig) und Troponin-spezifische Gene gehören. Die Bestimmung der genetischen Marker hat in diesem Zusammenhang auch prognostische Relevanz, da einige pathogene Varianten eine erhöhte Wahrscheinlichkeit für eine schlechtere Prognose und lebensbedrohliche Herzrhythmusstörungen nach sich ziehen können (beispielsweise bei LMNA und SCN5A).
- Arrhythmogene Kardiomyopathie (ACM): Bei dieser Variante lassen sich unter anderem Desmosom-Gene (kodieren für die mechanische Integrität des Herzgewebes zuständige Zellverbindungsproteine) als kritische Strukturen identifizieren. Das DGK-Papier nennt hier unter anderem PKP2 (Plakophilin 2), DSP (Desmoplakin), DSG2 (Desmoglein 2) und DSC2 (Desmocollin 2) [3].
Hinsichtlich der Interpretation des Befunds aus der Gensequenzierung steht mit der ACMG-Klassifikation (American College of Medical Genetics and Genomics) ein Schema zur Einteilung der Pathogenität gefundener Genvarianten zur Verfügung, welches die Varianten in fünf Kategorien einteilt.

Die Rolle genetischer Marker in Diagnostik und Behandlung
Wichtige Fakten auf einen Blick:
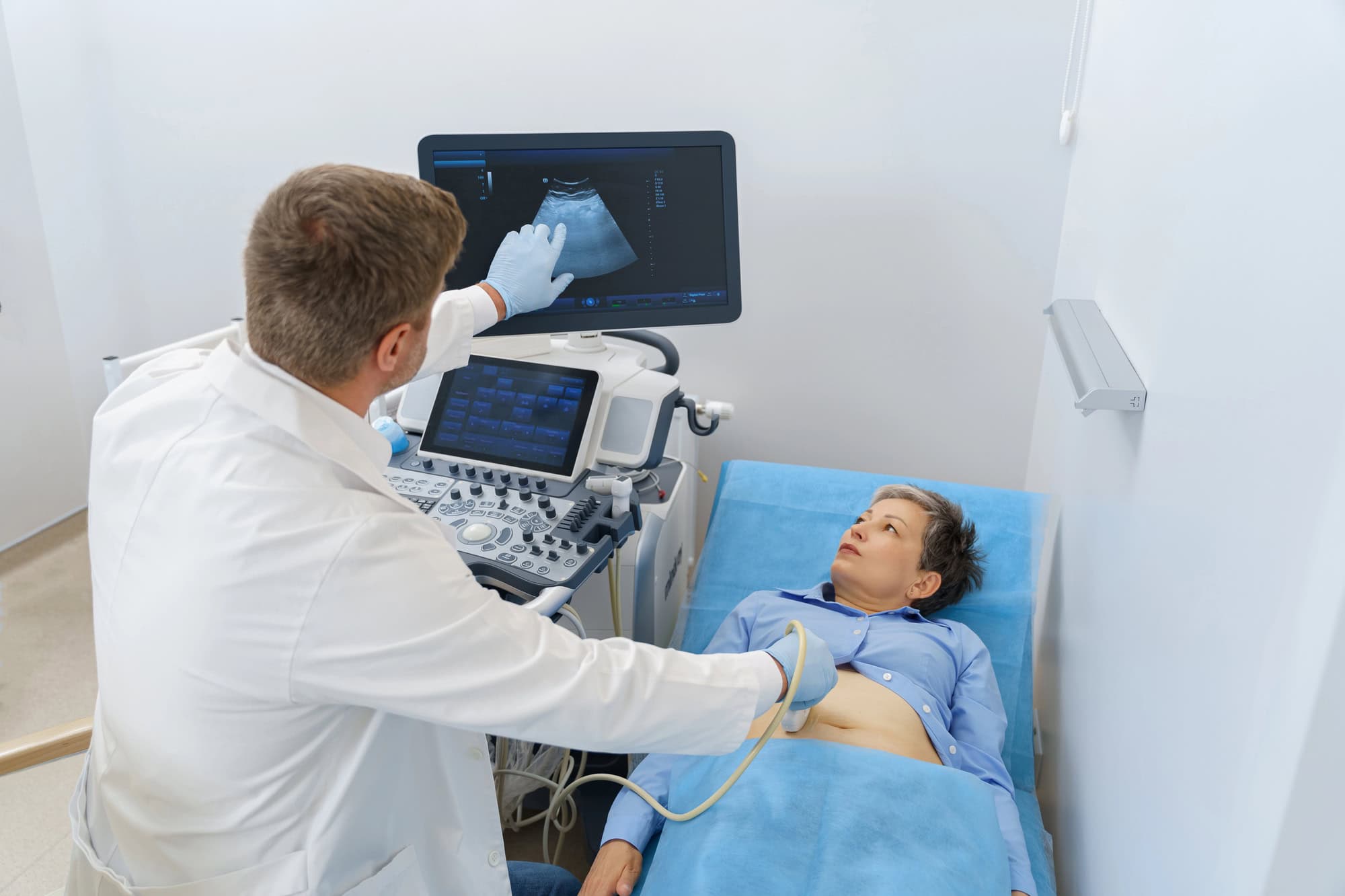
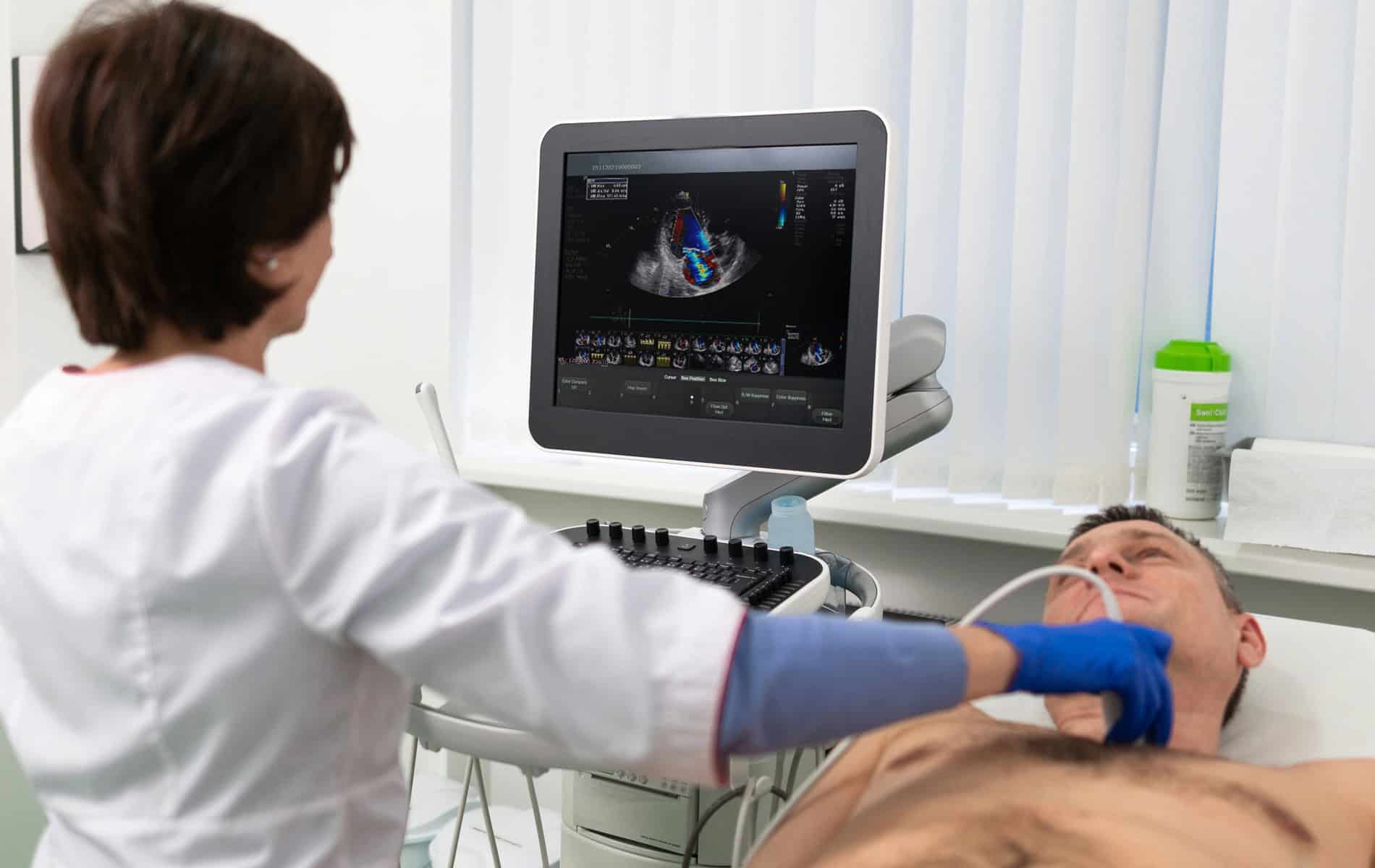
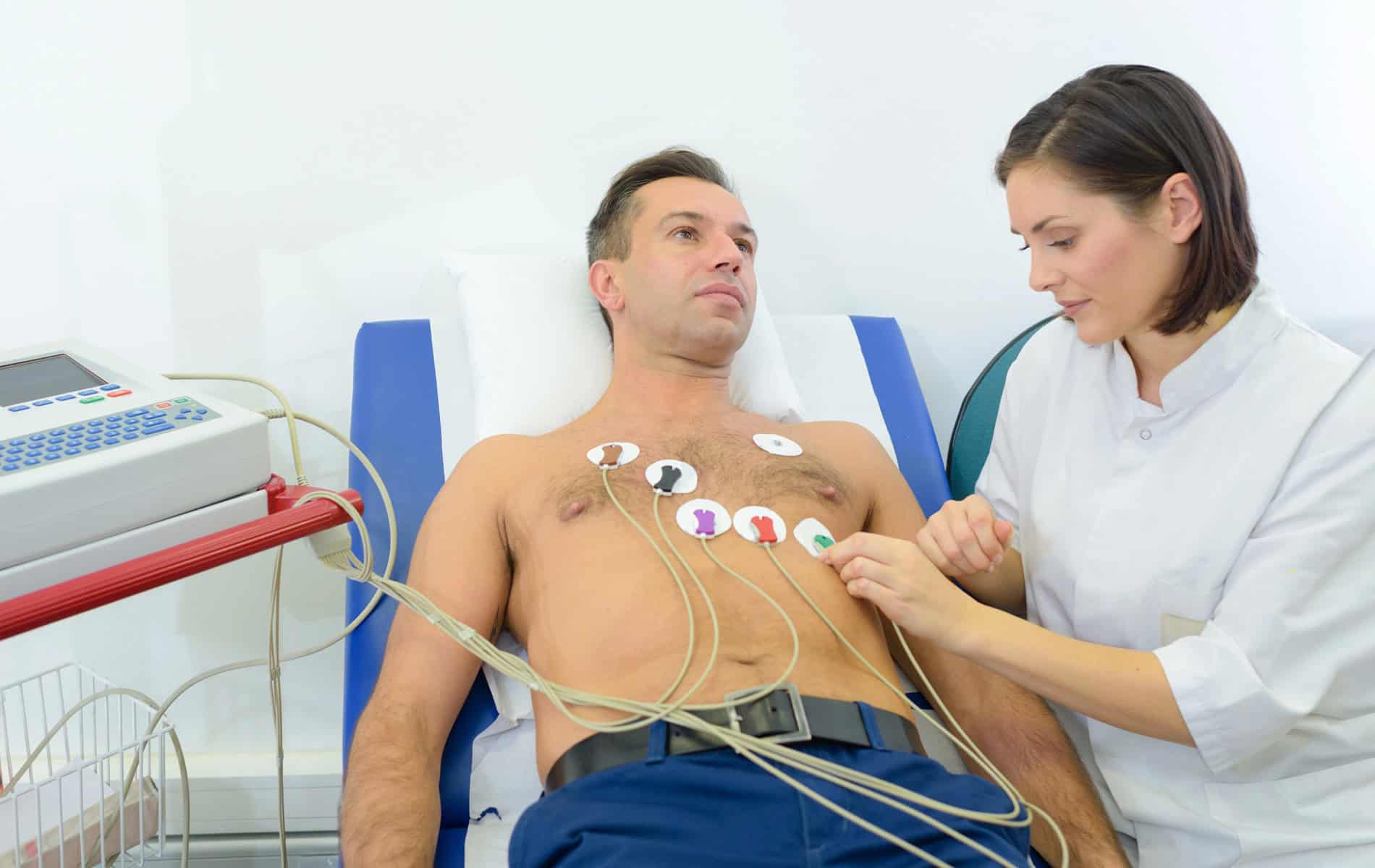
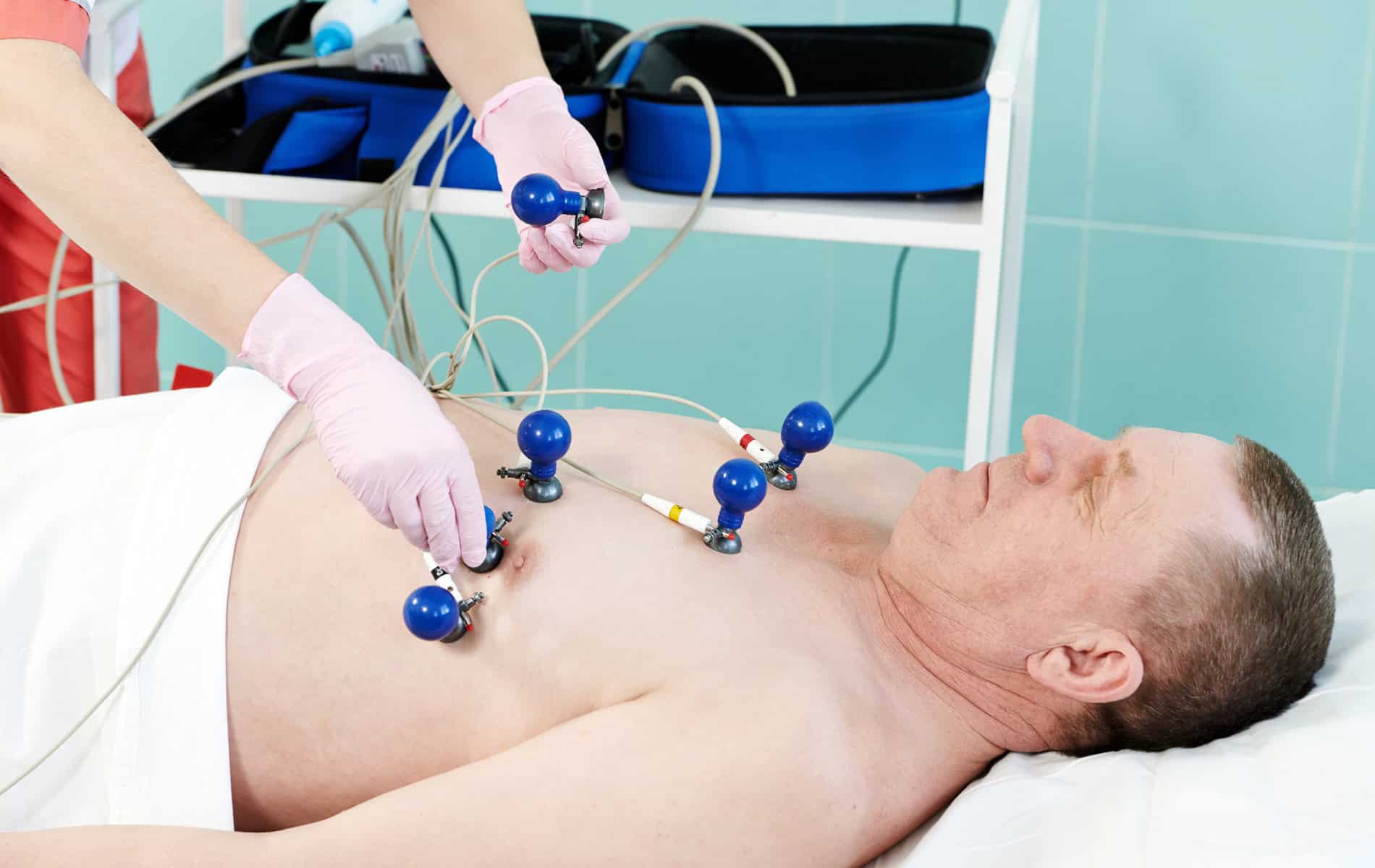
- Anamnese, Blutwerte und EKG sowie Herzultraschall bleiben wichtige Erstlinienuntersuchungen.
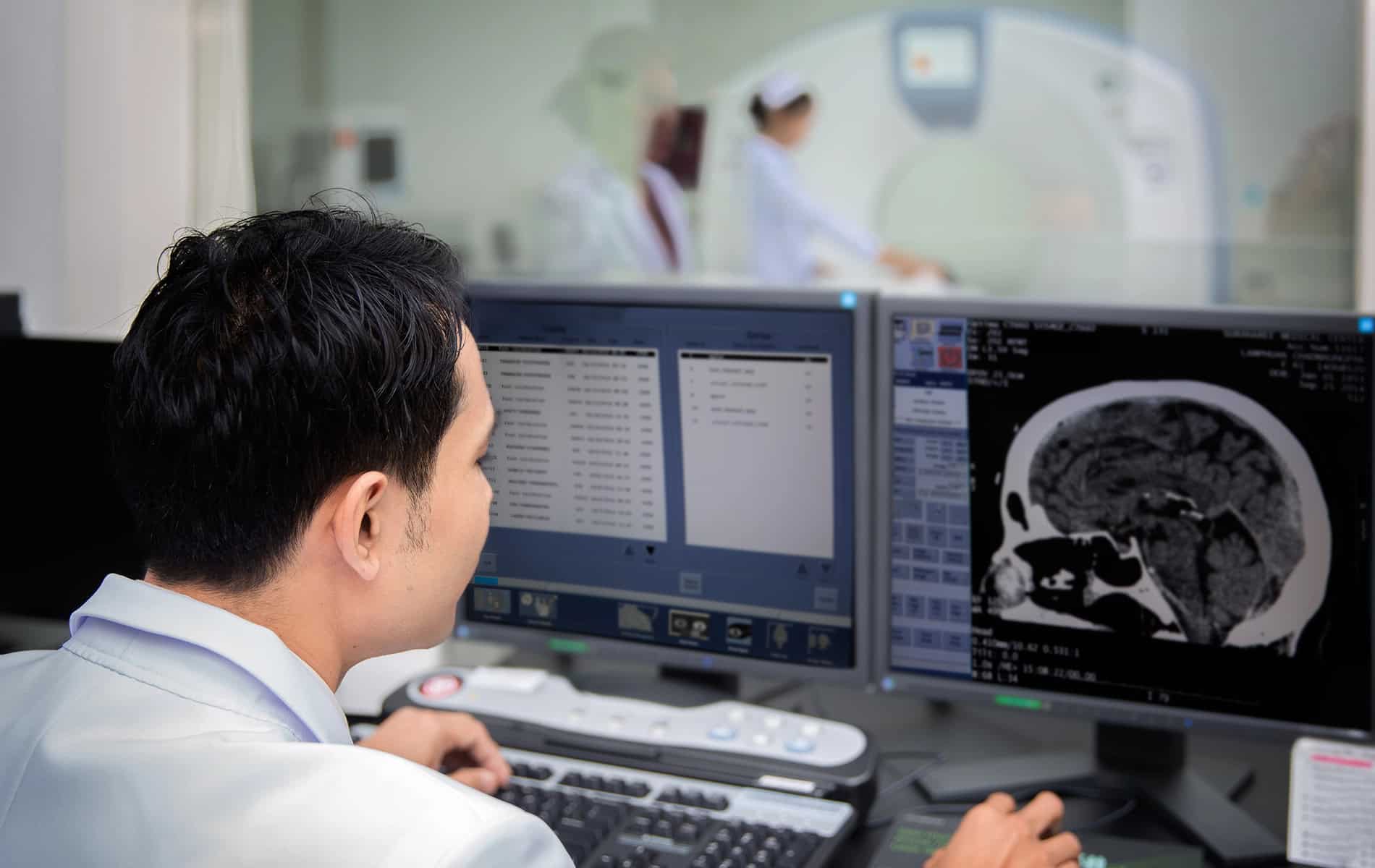
- Mithilfe der Bildgebung lässt sich das Herz funktionell und strukturell untersuchen.
- Die Gentests spielen für die Prognose, Therapieentscheidungen und Risikoabschätzung in der Familie eine Rolle.
Bei Verdacht auf das Vorliegen einer Kardiomyopathie umfasst die Diagnostik eine Kette verschiedener Verfahren, zu denen nicht nur genetische Marker gehören. Bei Betroffenen mit den genannten Symptomen werden zuerst die Anamnese und die körperliche Untersuchung zusammen mit Labortests (zur Bestimmung verschiedener Blutwerte) durchgeführt.
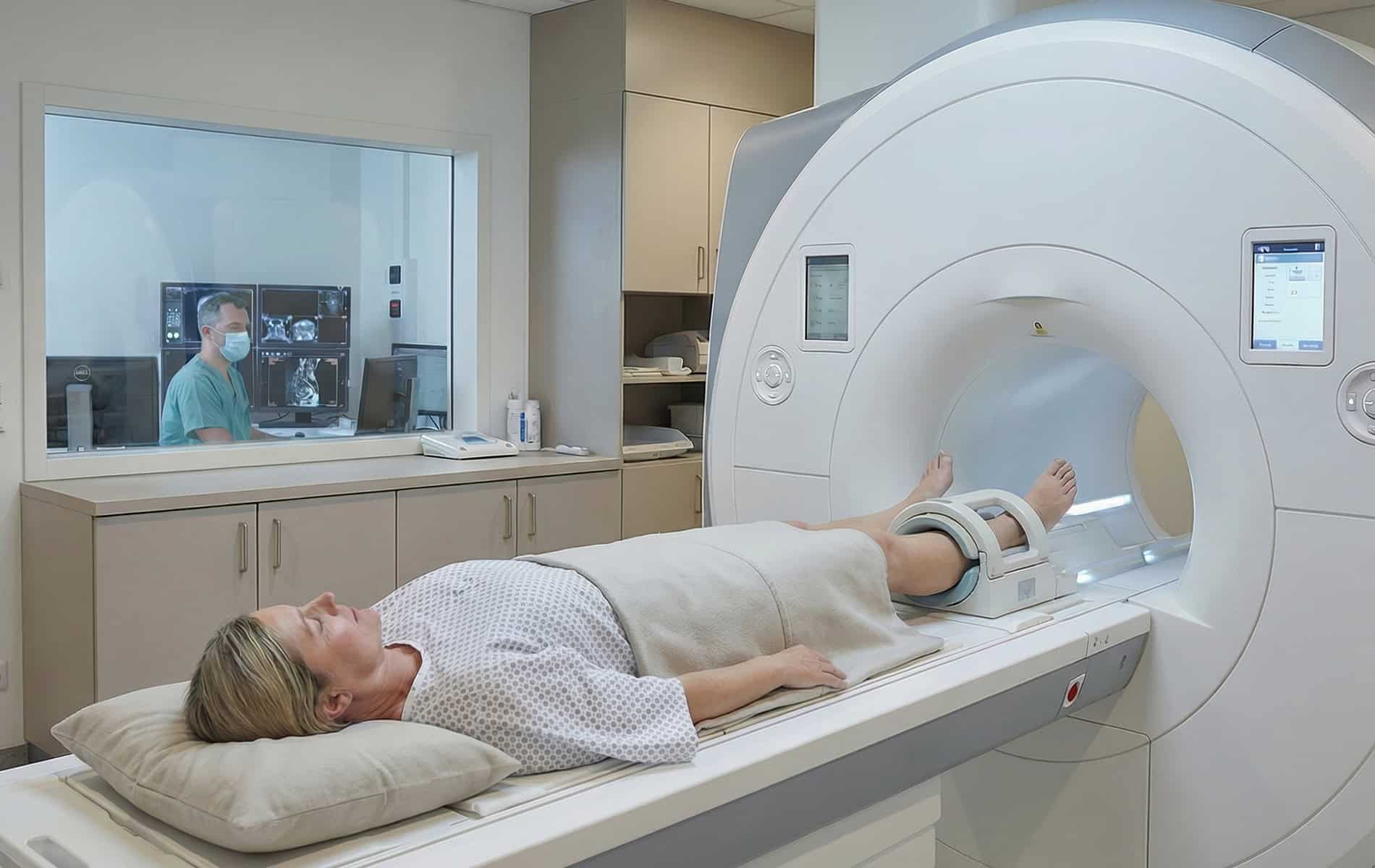
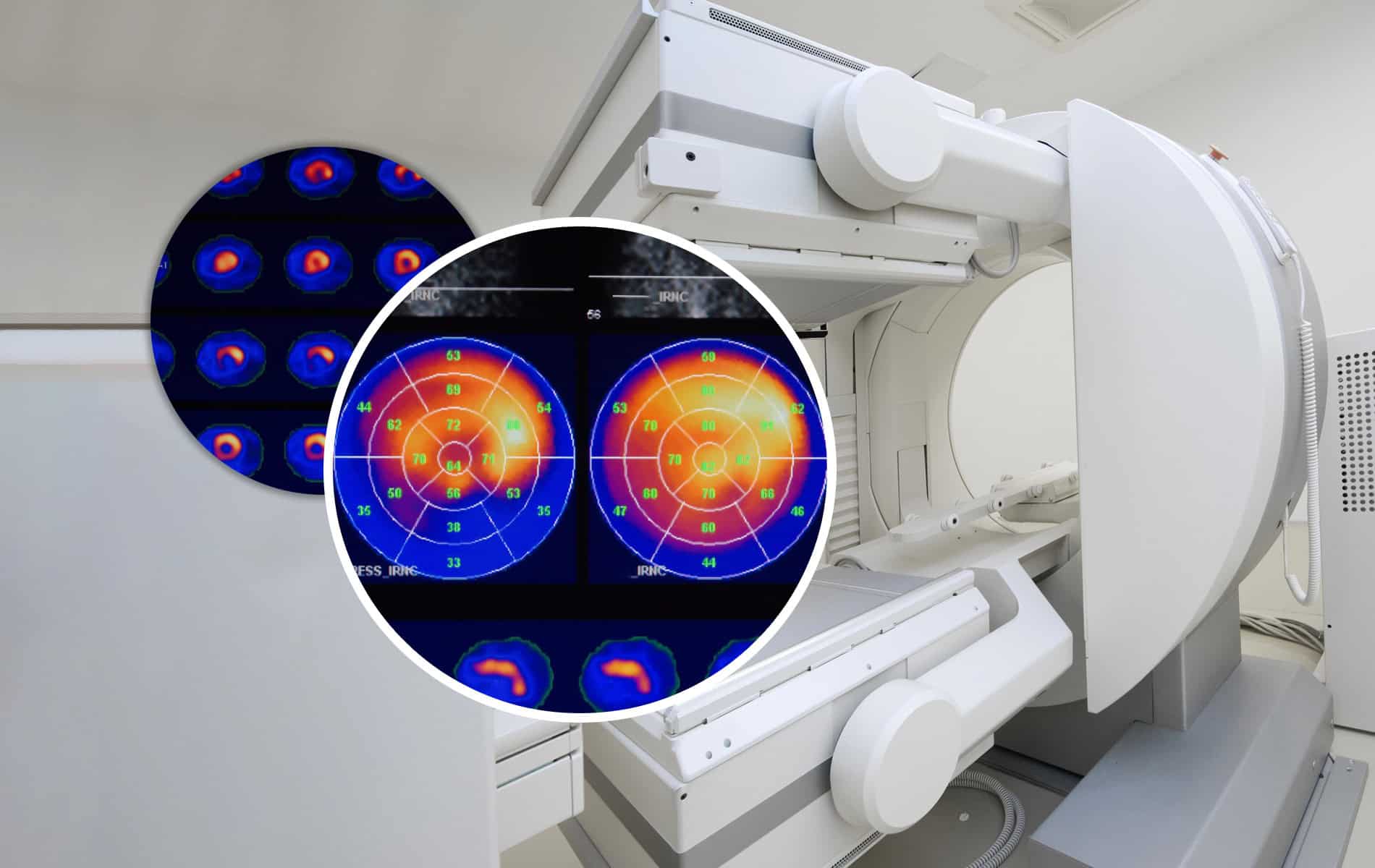
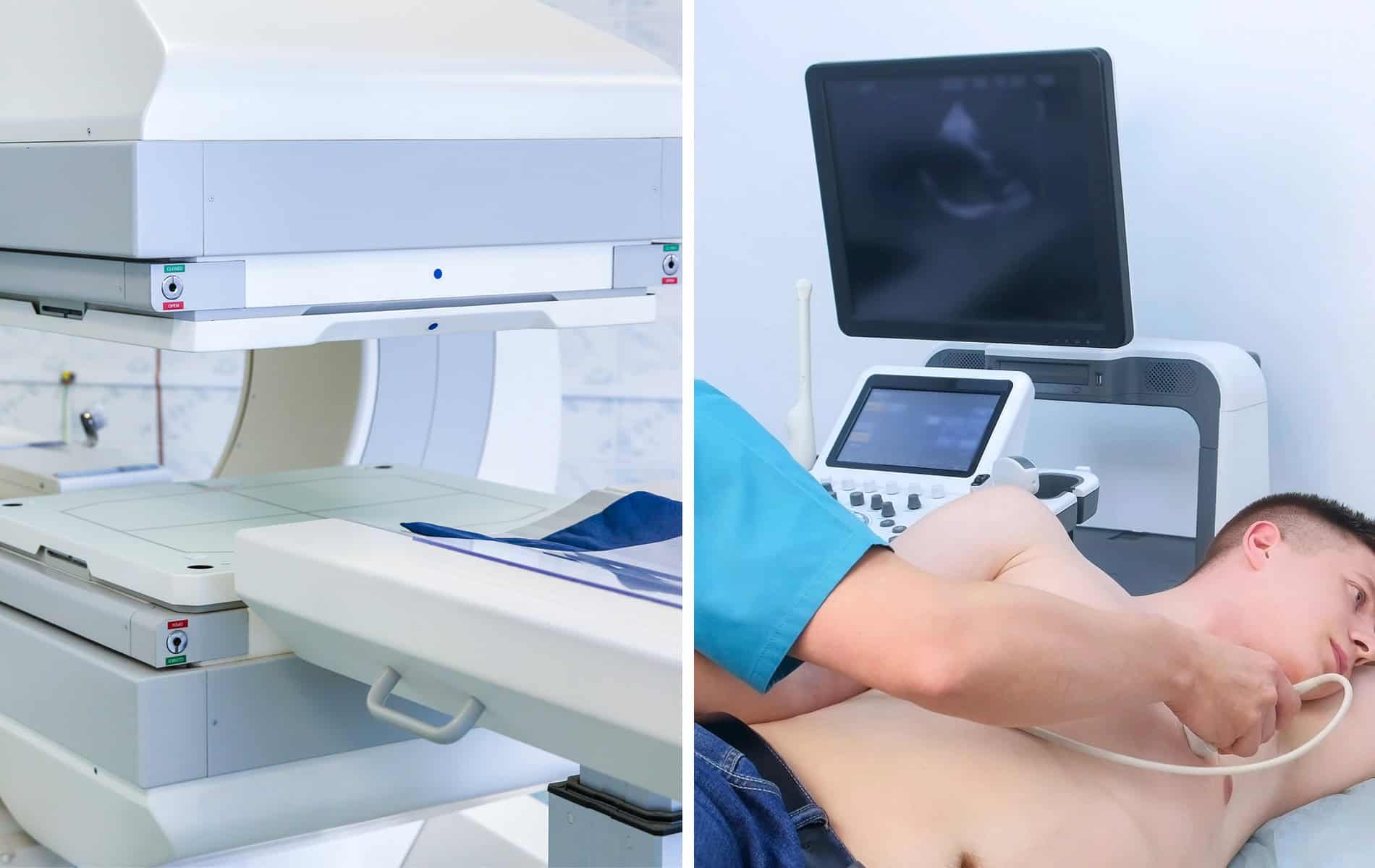
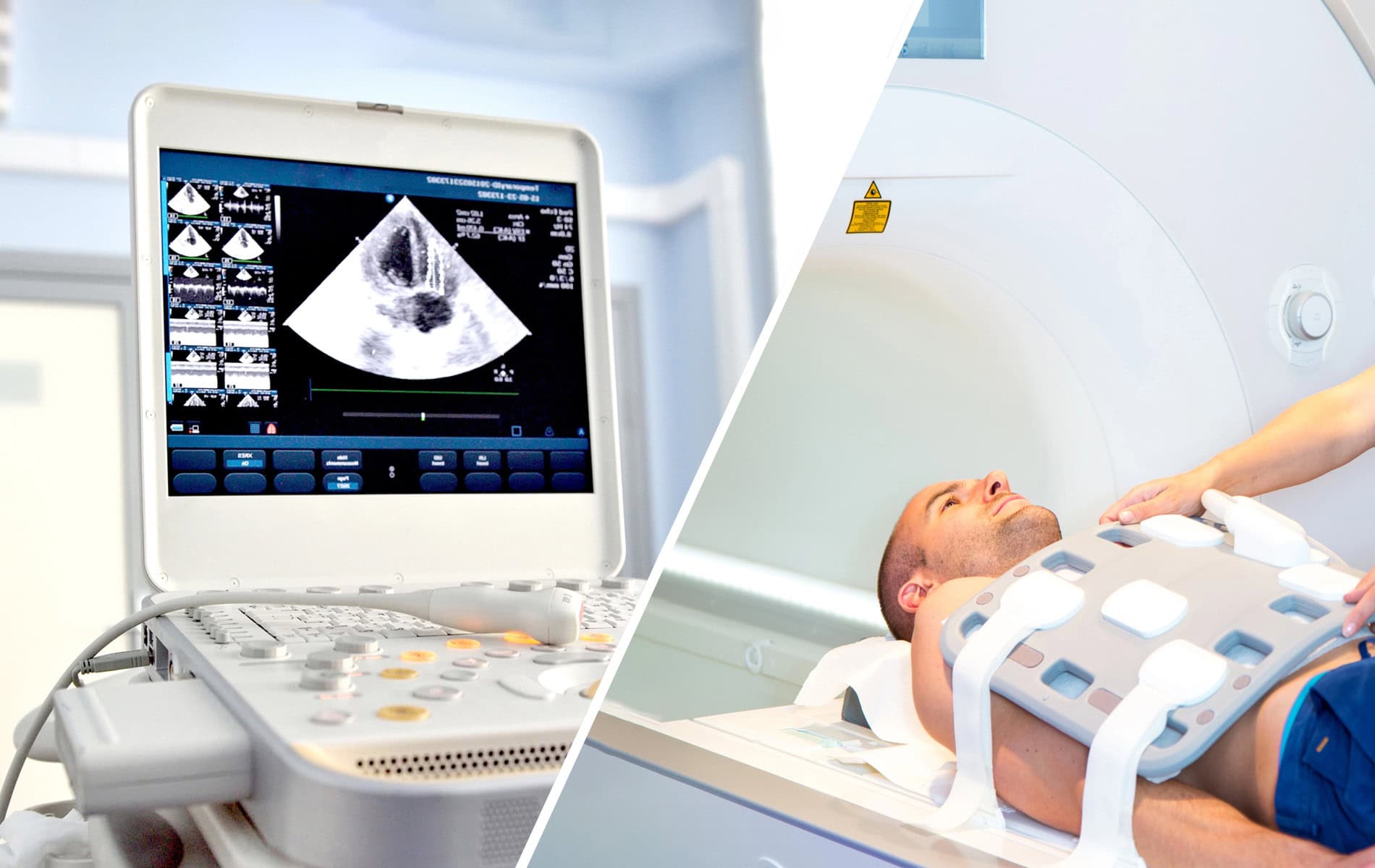
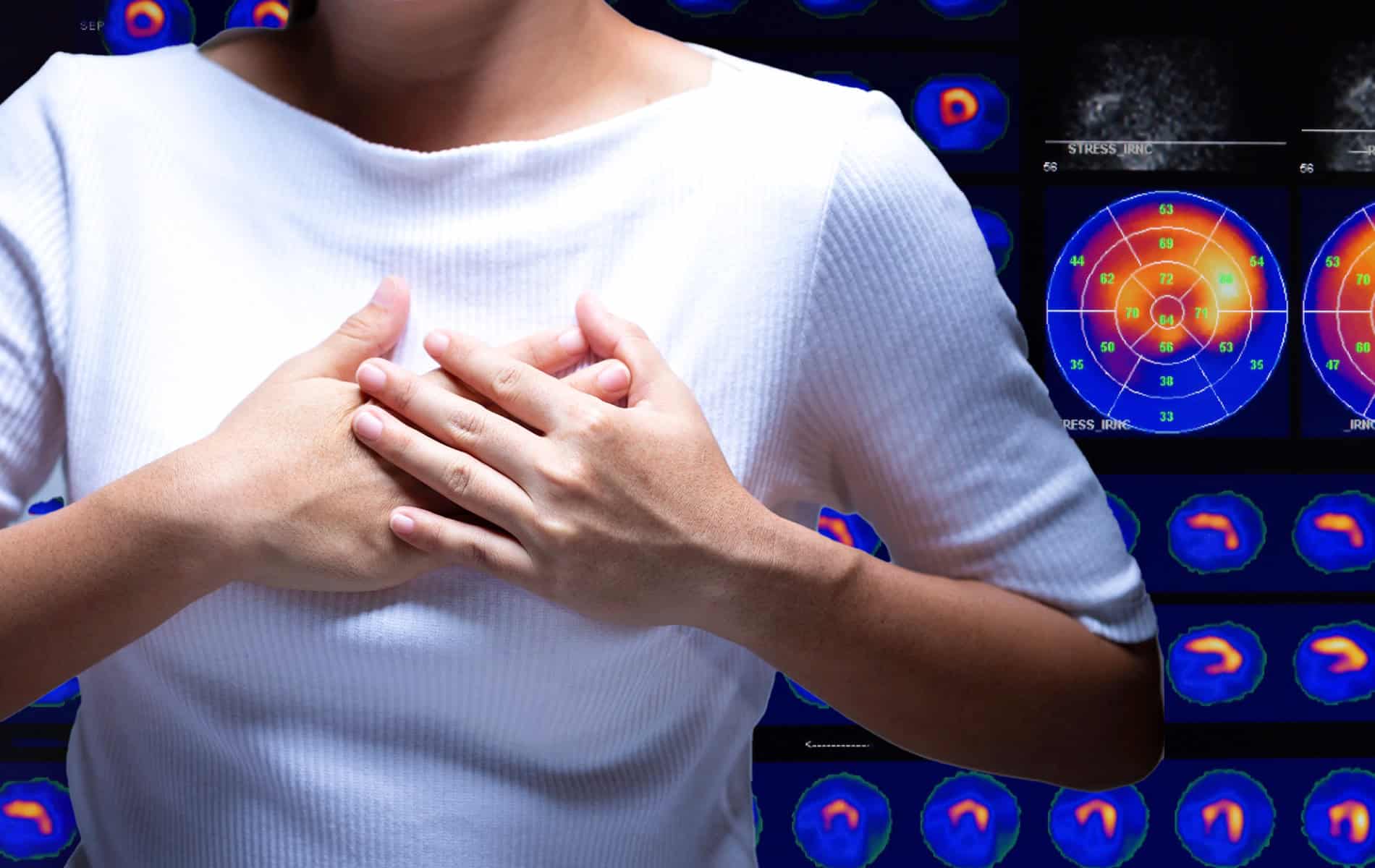
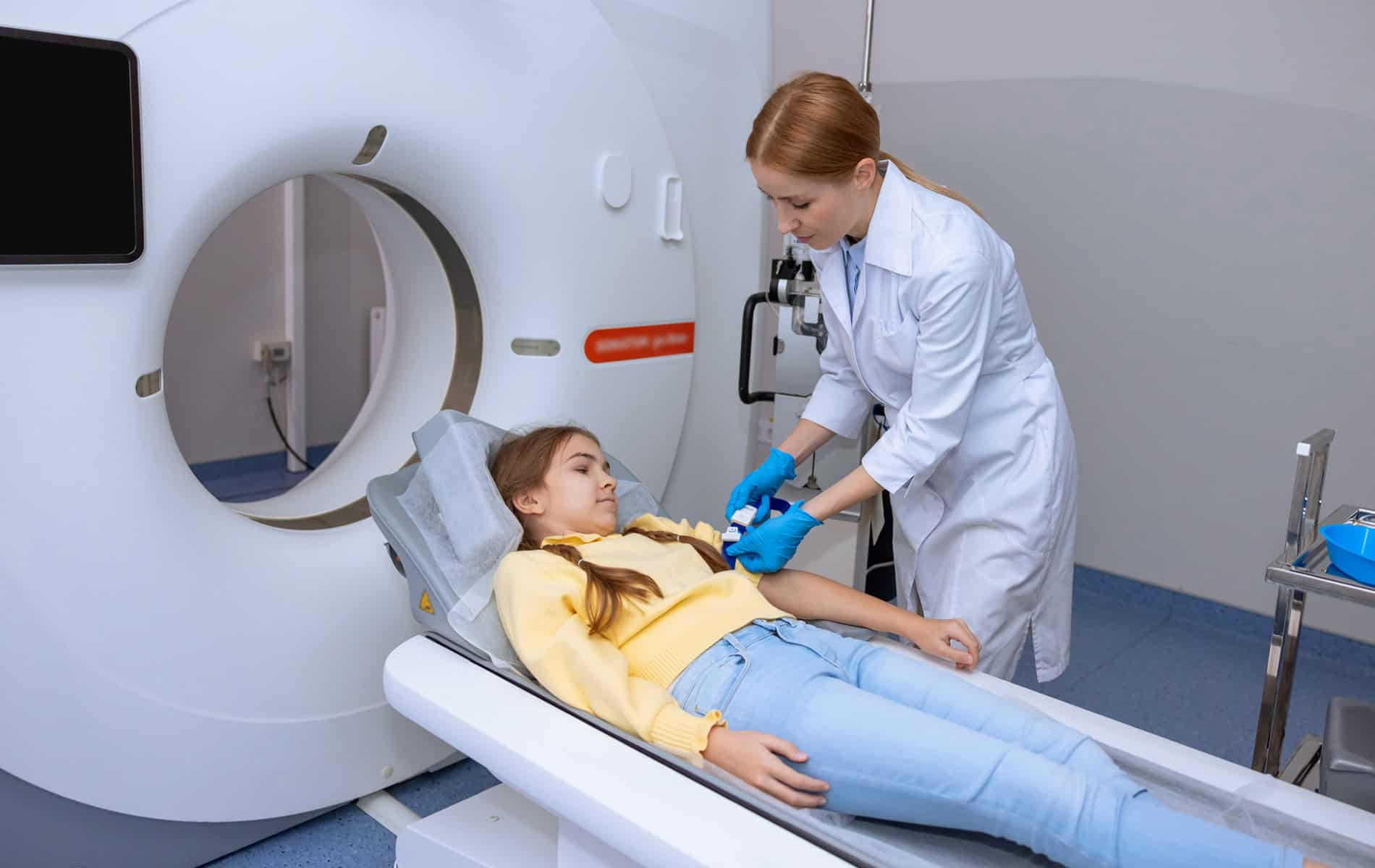
Dabei geht es um den Beginn der Symptome, einen Zusammenhang mit Infektionen, die Familienanamnese und die Testung wichtiger kardiologischer Marker – da Atemnot und Synkopen auch bei anderen Herzerkrankungen auftreten. Weiterhin spielen in der Diagnostik das Elektrokardiogramm (EKG), die Echokardiographie (Herzultraschall) sowie die Kardio-MRT, Szintigraphien und die Myokardbiopsie eine Rolle.
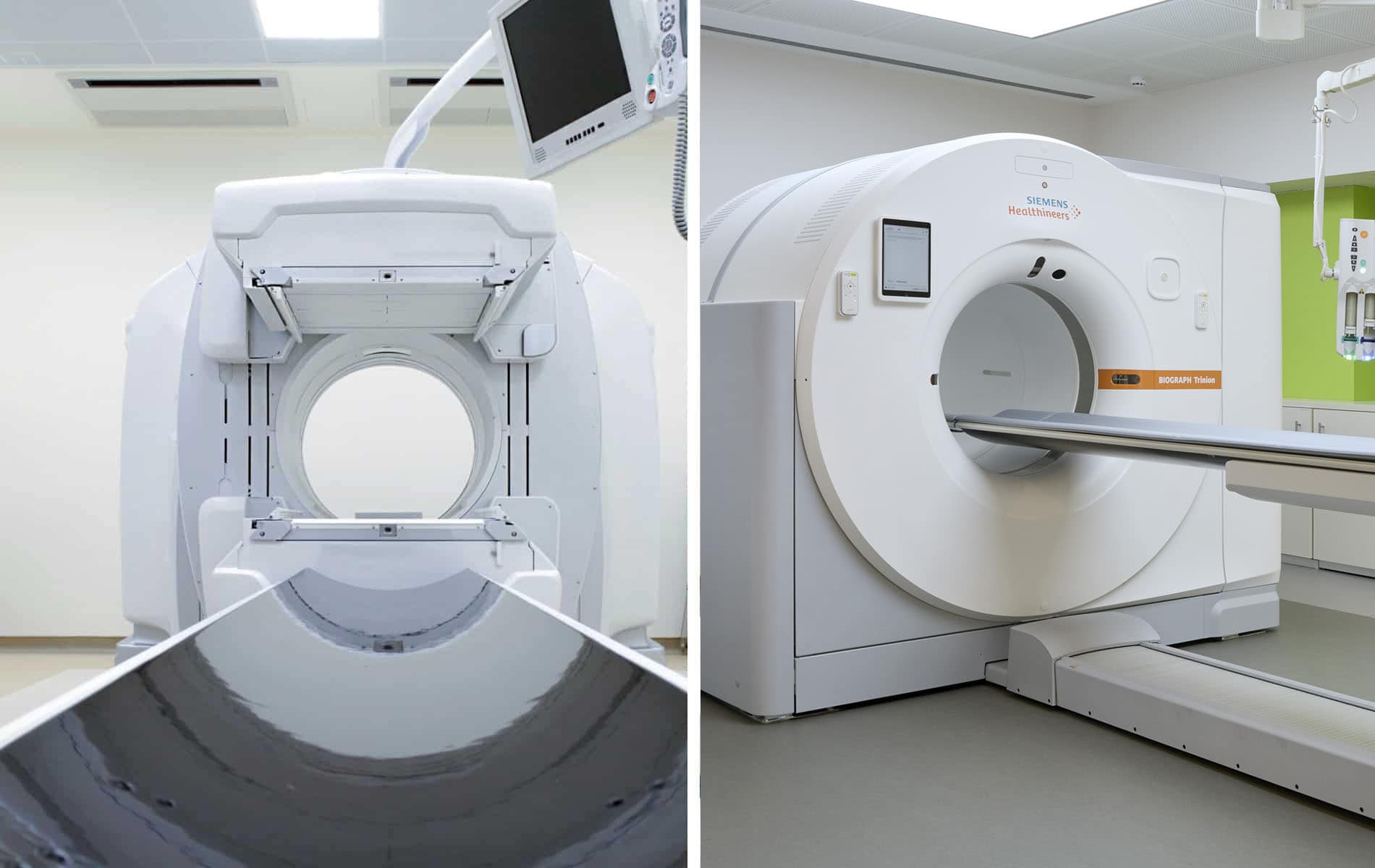
Die PET-Untersuchung (Positronen-Emissions-Tomographie) kommt in der kardialen Diagnostik bei spezifischen Fragestellungen zum Einsatz, da die Kombination aus PET und radiologischen Bildgebungsverfahren eine umfassende myokardiale Gewebecharakterisierung erlaubt. So liefert die Magnetresonanztomographie (MRT) zum Beispiel strukturelle Informationen, während mit der PET aktive myokardiale Entzündungsprozesse identifiziert werden können.
Genetische Tests gehören nicht zu den Erstlinienverfahren, sondern werden als Ergänzung angesehen – sowohl im Hinblick auf die Prognose als auch für die Familienevaluation. Sie ermöglichen eine intensive Suche nach den Grundlagen der Kardiomyopathie (Vererbungsmodus und Heterogenität). Zudem bietet dieser Ansatz die Möglichkeit, weitere Risikopersonen im Familienkreis ausfindig zu machen.
Darüber hinaus ist Kenntnis des Genotyps auch aus therapeutischer Sicht relevant, denn bei Patienten mit einer ACM besteht ein erhöhtes Risiko schwerer kardialer Komplikationen wie dem plötzlichen Herztod. Der Klassifizierung der Variante durch Gentests kommt damit besondere Bedeutung bei, da ein Kardioverter-Defibrillator (ICD) als Implantat den zentralen Schutzmechanismus gegen diese Gefahr darstellt [4].
Genetische Marker als Pfeiler zukünftiger kardiologischer Untersuchungen
Angesichts der Fortschritte wird die Bedeutung genetischer Marker in Zukunft voraussichtlich weiter zunehmen. Gerade die präzise Identifikation pathogener Genvarianten kann eine wachsende Rolle für Therapiestrategien, das Familienscreening und die eigentliche Diagnostik spielen. Denkbar ist ein Ansatz, bei dem Genom-Informationen mit spezifischen Tracern – schwach radioaktiv markierte Verbindungen, die an bestimmte Strukturen binden – zur Durchführung bildgebender Verfahren verknüpft werden. An dieser Genom-basierte Bildgebung arbeiten Forscher unter anderem mit Verfahren wie der PET-CT [5]. Zugleich kann der Ansatz, genetische Marker zu verwenden, im Rahmen der Liquid Biopsy (Untersuchungen von Blutproben auf zirkulierende DNA-Fragmente) die Früherkennung bei asymptomatischen Risikopersonen verbessern.
Mehr über LifeLink
Finden Sie jetzt die
Praxis in Ihrer Nähe!
Wir sind überzeugt, dass die Medizin von morgen anders aussehen sollte. Wir sehen den Menschen im Mittelpunkt exzellenter Medizin.
Fazit: Die Bedeutung von Genmarkern in der Diagnostik nimmt zu
Kardiomyopathien treten mit einem Spektrum sehr unterschiedlicher Symptome auf, was die Diagnostik erschwert. In der Herzmedizin (Kardiologie) wird diesbezüglich nach wie vor auf eine Kombination verschiedener bildgebender Untersuchungsverfahren gesetzt. Jedoch gewinnen Genmarker an Bedeutung, da sie nicht nur für die Abgrenzung der einzelnen Varianten voneinander und anderen Erkrankungen relevant sind. Mit ihrer Hilfe lassen sich Aussagen zur Prognose treffen und therapeutische Entscheidungen stützen. Aller Voraussicht nach können Untersuchungen auf spezifische Genmutationen in Zukunft ein noch präziseres Arbeiten in der Herzmedizin ermöglichen.
FAQ zur Untersuchung von Kardiomyopathien mit Genmarkern: Die wichtigsten Fragen und Antworten
Wie lange dauert eine genetische Analyse und was kostet sie?
Moderne Untersuchungen in spezialisierten humangenetischen Laboren dauern in der Regel drei bis sechs Wochen. Hinsichtlich der Kosten ist entscheidend, ob auf einzelne Mutationen oder ein komplettes Panel, also eine größere Anzahl von Genen, getestet wird.
Hat jeder Patient Anspruch auf eine Genom-Untersuchung?
Der Anspruch besteht nur unter bestimmten Voraussetzungen, nämlich wenn spezifische Formen der Kardiomyopathie vermutet werden. Dies kann bei einem plötzlichen Herztod in der Familie der Fall sein. Diese Gentests sollen weitere Risikopersonen identifizieren und Komplikationen vermeiden helfen.
Muss bei einer Genmutationen immer ein Schrittmacher oder ein Defibrillator implantiert werden?
Nein, nicht jede der heute in der Molekularmedizin und Kardiologie bekannten Mutationen erhöht das Risiko für Patienten. Einige der Gendefekte sind gutartig, sodass von diesen – nach heutigem Kenntnisstand – keine klinische Relevanz oder ein erhöhtes Risiko ausgeht. Bei kritischen Genmutationen kommt die Implantation eines Schrittmachers oder Defibrillators indes in Betracht.
[1] Pinamonti B, Brun F, Mestroni L, Sinagra G. Arrhythmogenic right ventricular cardiomyopathy: From genetics to diagnostic and therapeutic challenges. World J Cardiol. 2014 Dec 26;6(12):1234-44. doi: 10.4330/wjc.v6.i12.1234. PMID: 25548613; PMCID: PMC4278158.
[2] Sadasivan C, Gagnon LR, Hazra D, Wang K, Youngson E, Thomas J, Chan AYM, Paterson DI, McAlister FA, Dzwiniel T, Tymchak W, Christian S, Oudit GY. Early genetic screening and cardiac intervention in patients with cardiomyopathies in a multidisciplinary clinic. ESC Heart Fail. 2025 Jun;12(3):1942-1955. doi: 10.1002/ehf2.15202. Epub 2024 Dec 30. PMID: 39740200; PMCID: PMC12055407.
[3] Schulze-Bahr, E., Klaassen, S., Gerull, B. et al. Gendiagnostik bei kardiovaskulären Erkrankungen. Kardiologie 17, 300–349 (2023), Seite 304. https://doi.org/10.1007/s12181-023-00622-3
[4] Schulze-Bahr, E., Klaassen, S., Gerull, B. et al. Gendiagnostik bei kardiovaskulären Erkrankungen. Kardiologie 17, 300–349 (2023); Seite 323. https://doi.org/10.1007/s12181-023-00622-3
[5] Jané, P., Xu, X., Taelman, V. et al. The Imageable Genome. Nat Commun 14, 7329 (2023). https://doi.org/10.1038/s41467-023-43123-3