Radioresistenz überwinden: Neue Strategien gegen therapieresistente Tumore
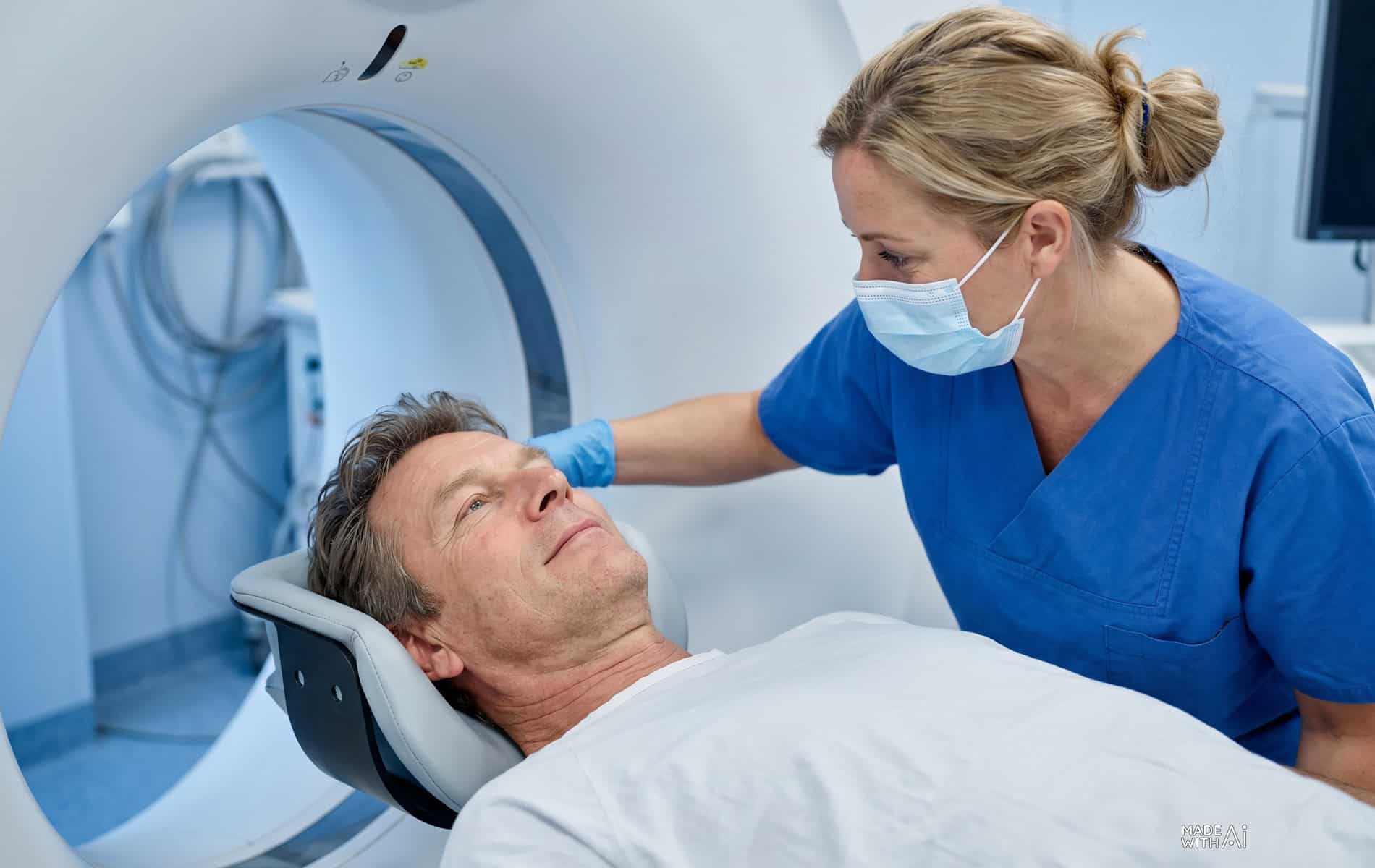
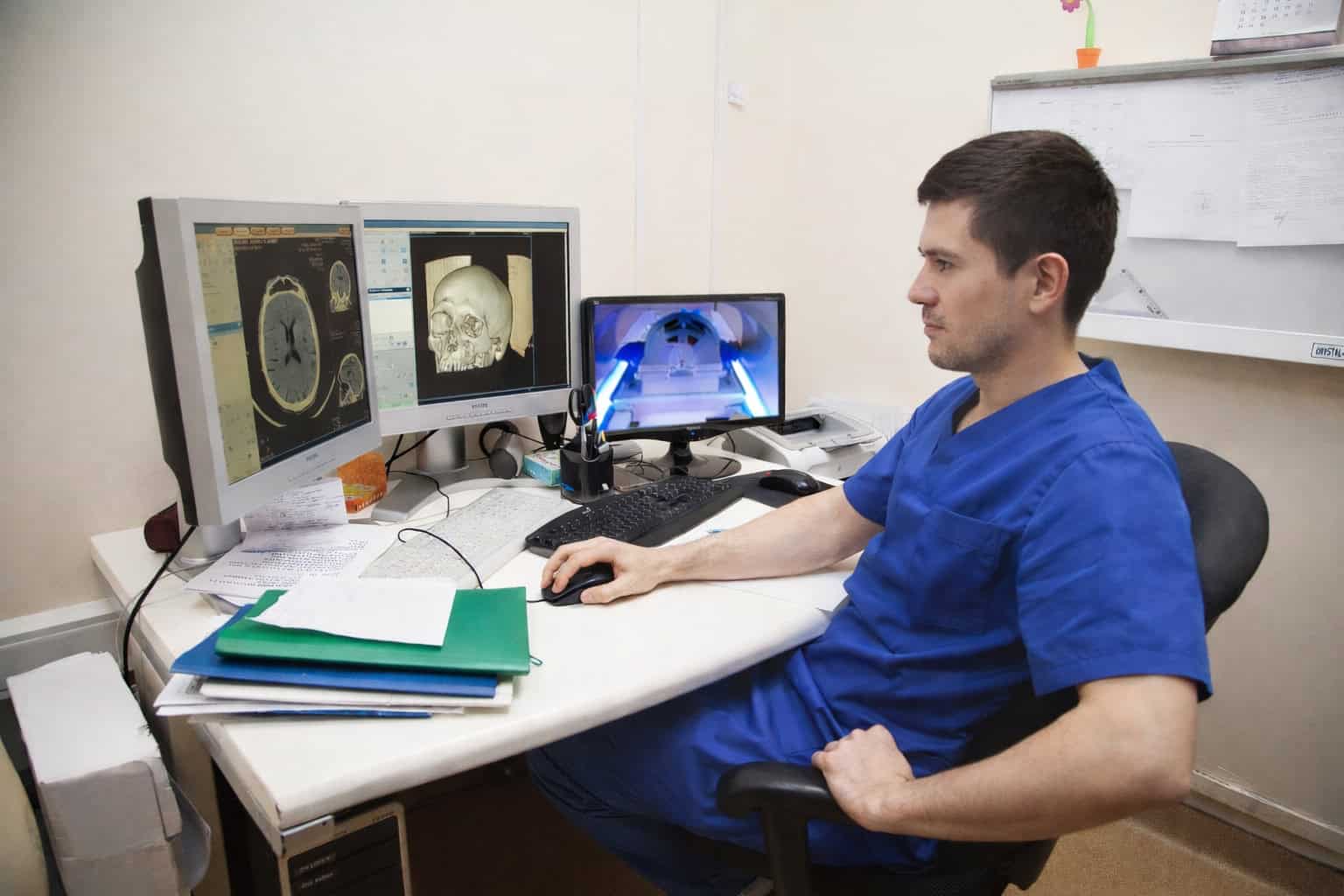
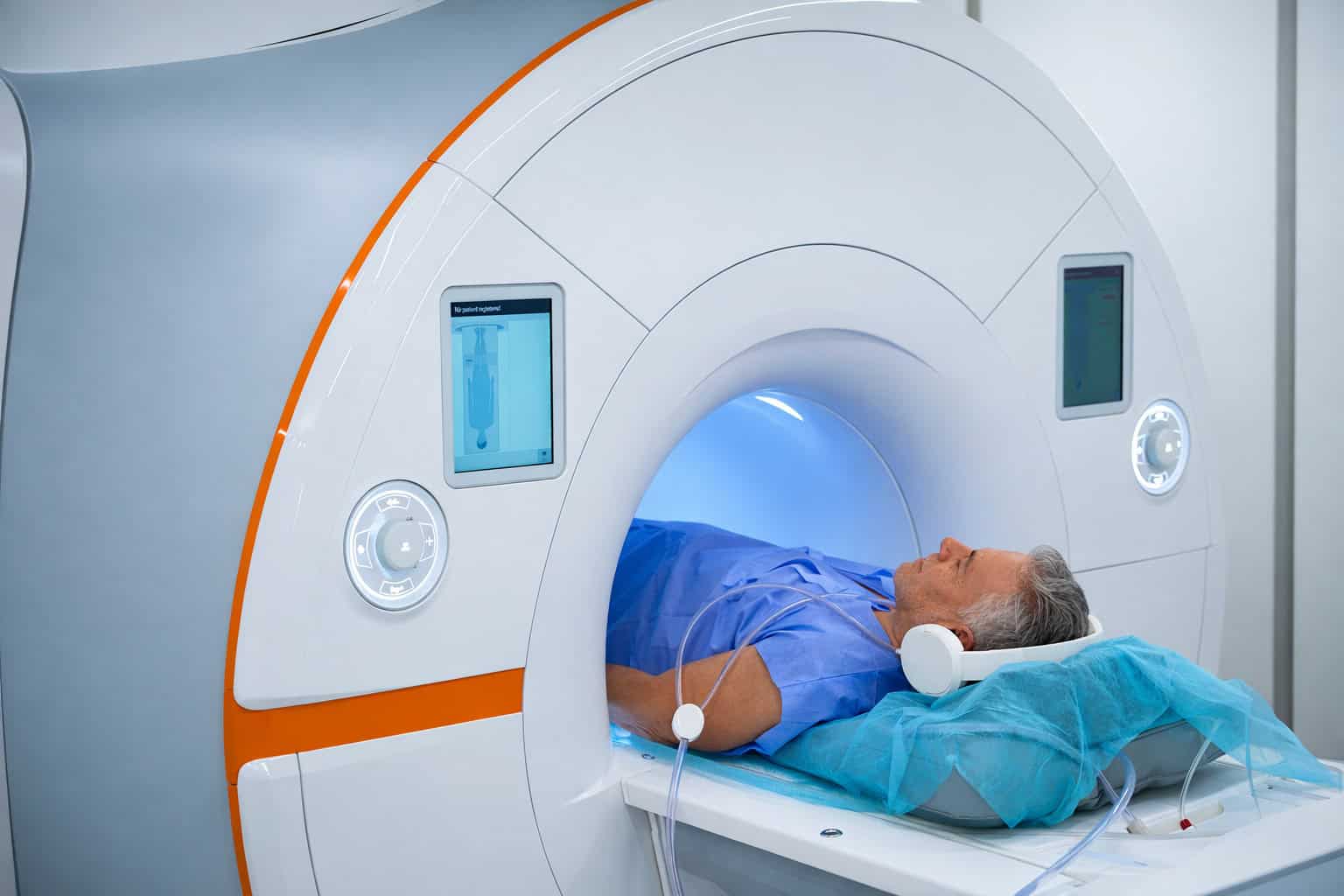
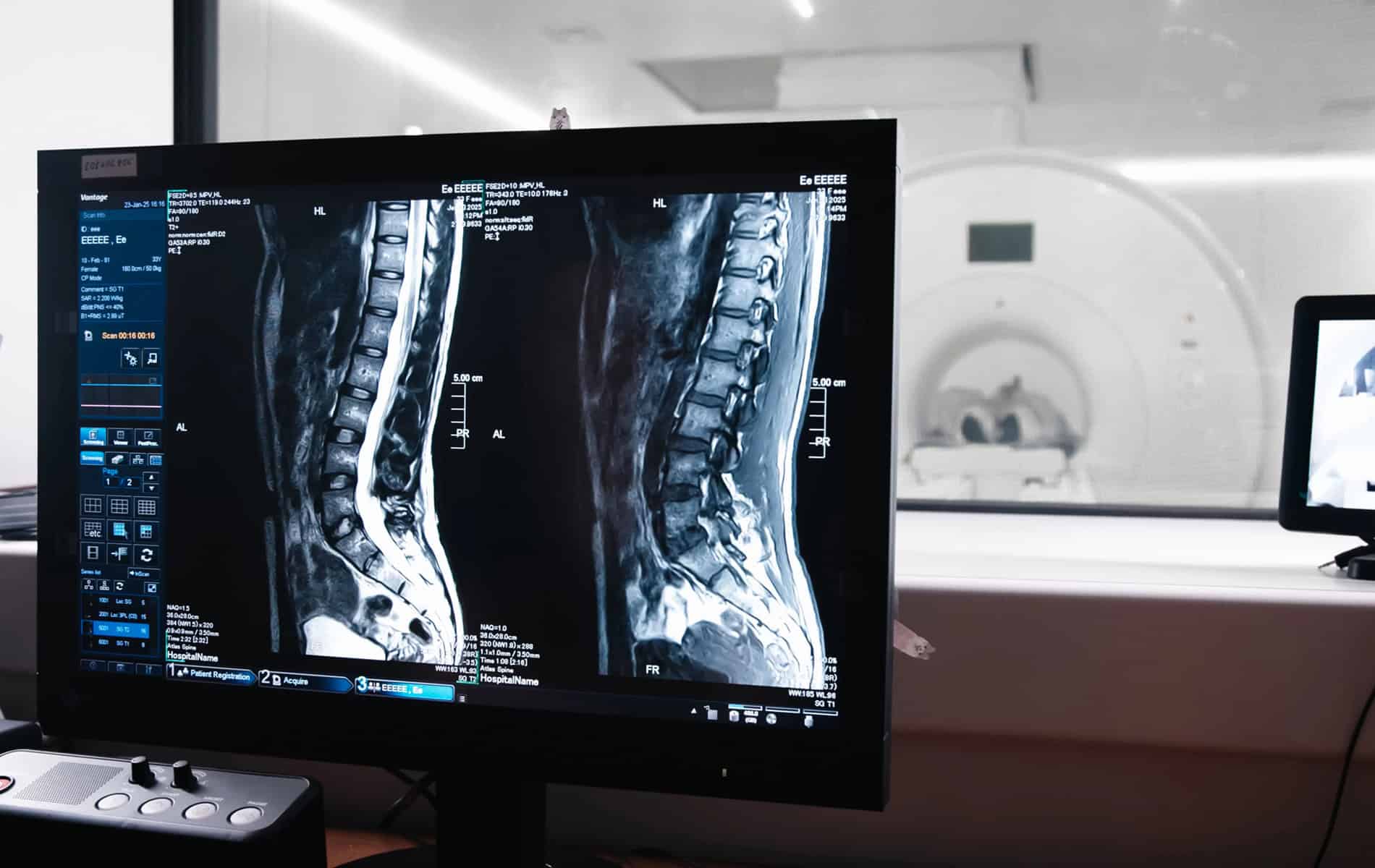
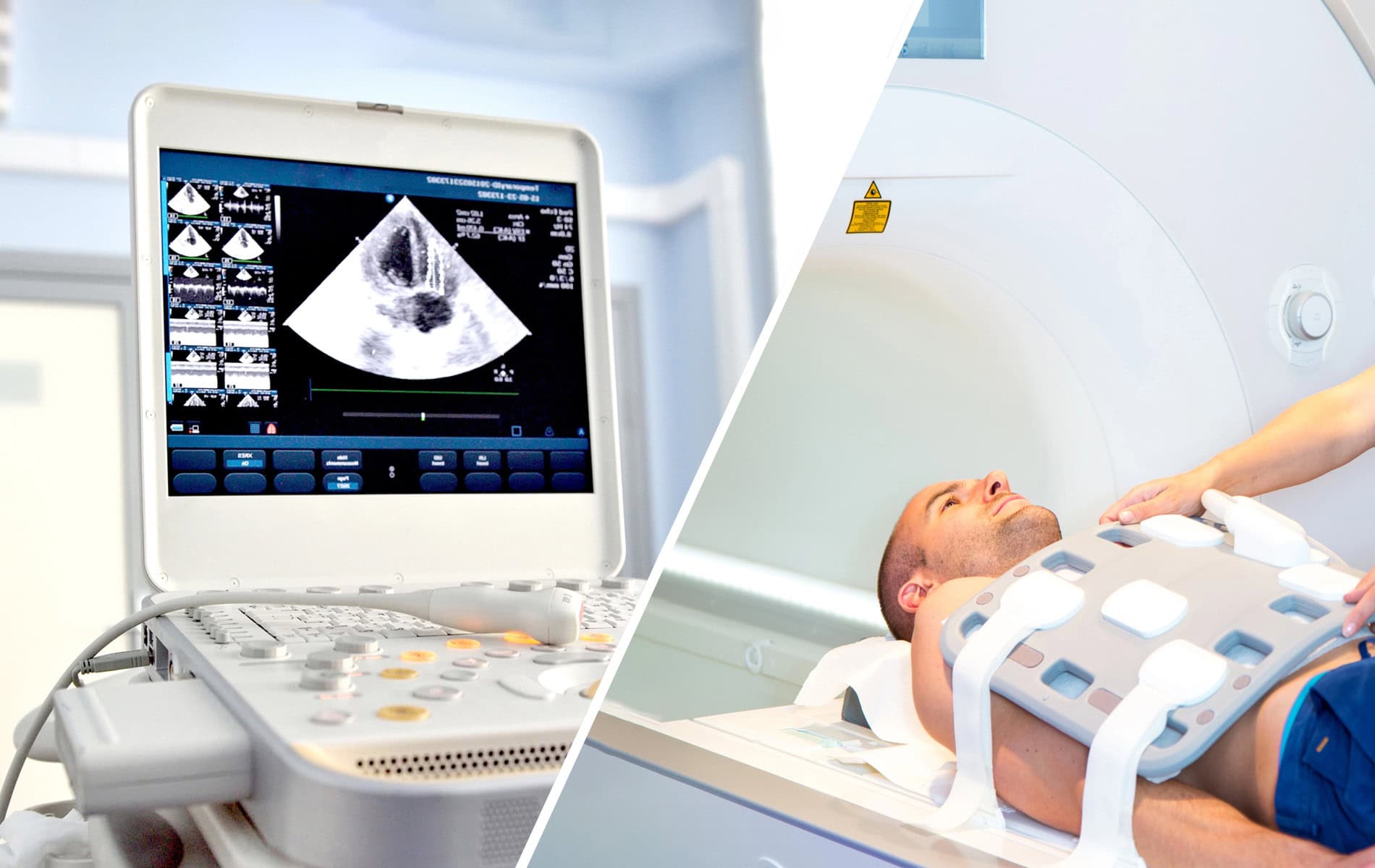
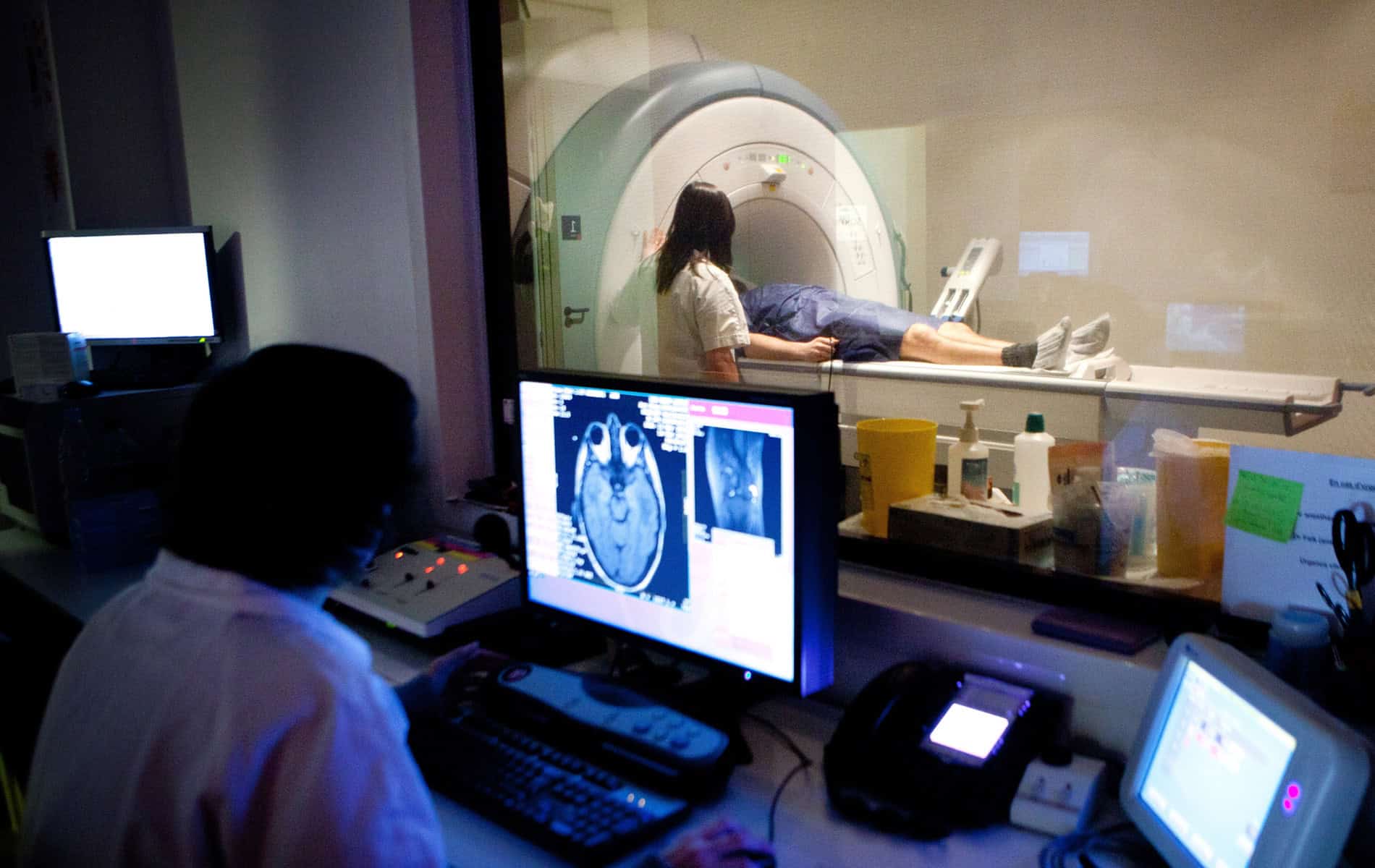
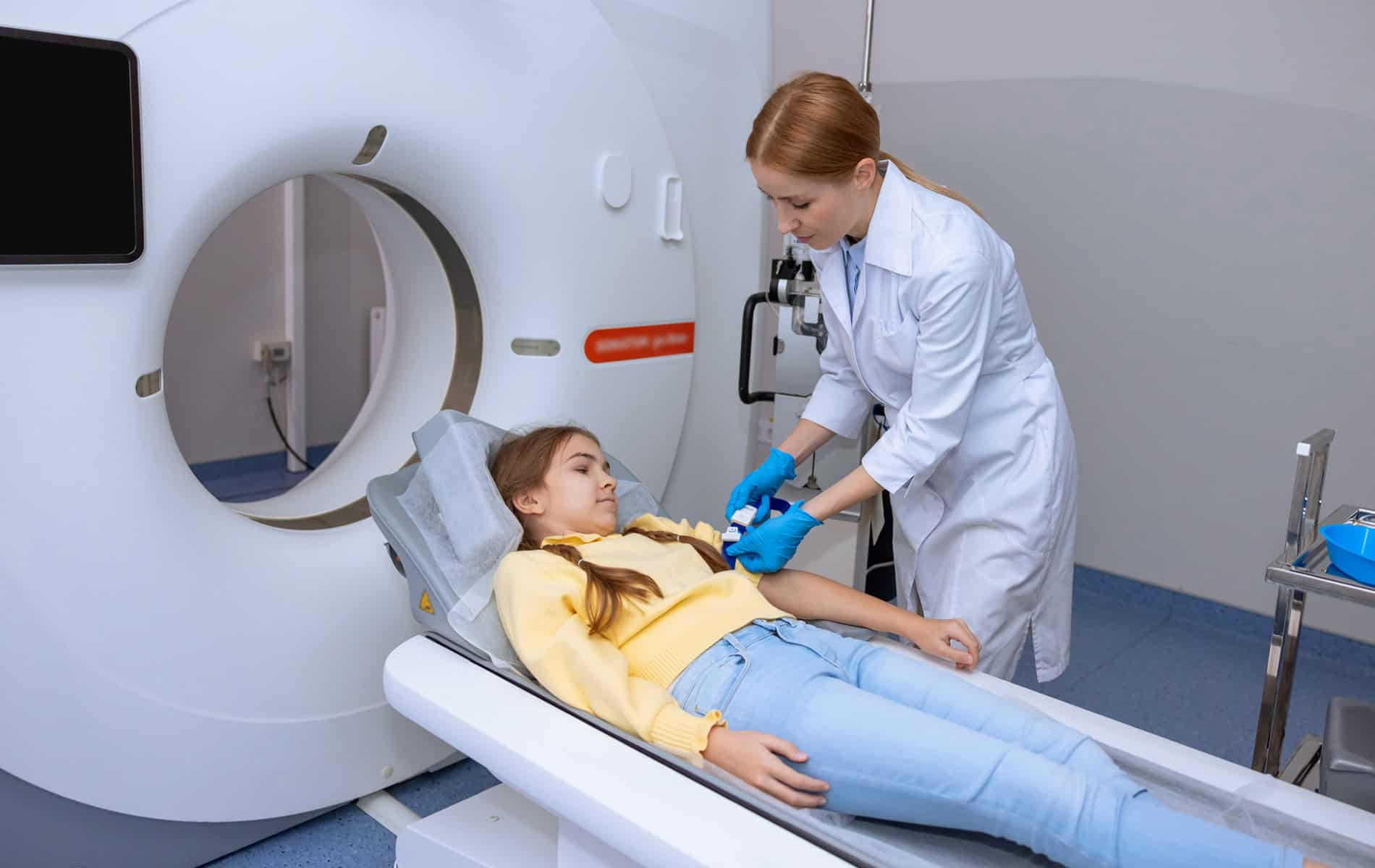
In der Krebsmedizin (Onkologie) nimmt die Strahlentherapie eine bedeutende Rolle ein und hat sich zu einer tragenden Säule verschiedener Behandlungsansätze entwickelt. Etwas mehr als die Hälfte der Krebspatienten erhält eine Bestrahlung. Die Therapiemethode macht sich dabei die toxische Wirkung der Strahlung auf Gewebe zunutze (ionisierende Strahlung verursacht DNA-Schäden), um Krebszellen zu zerstören. Trotz technologischer Fortschritte in der Bestrahlungsplanung und Durchführung bleibt die Radioresistenz (Strahlenresistenz) eine Herausforderung in der Radioonkologie.
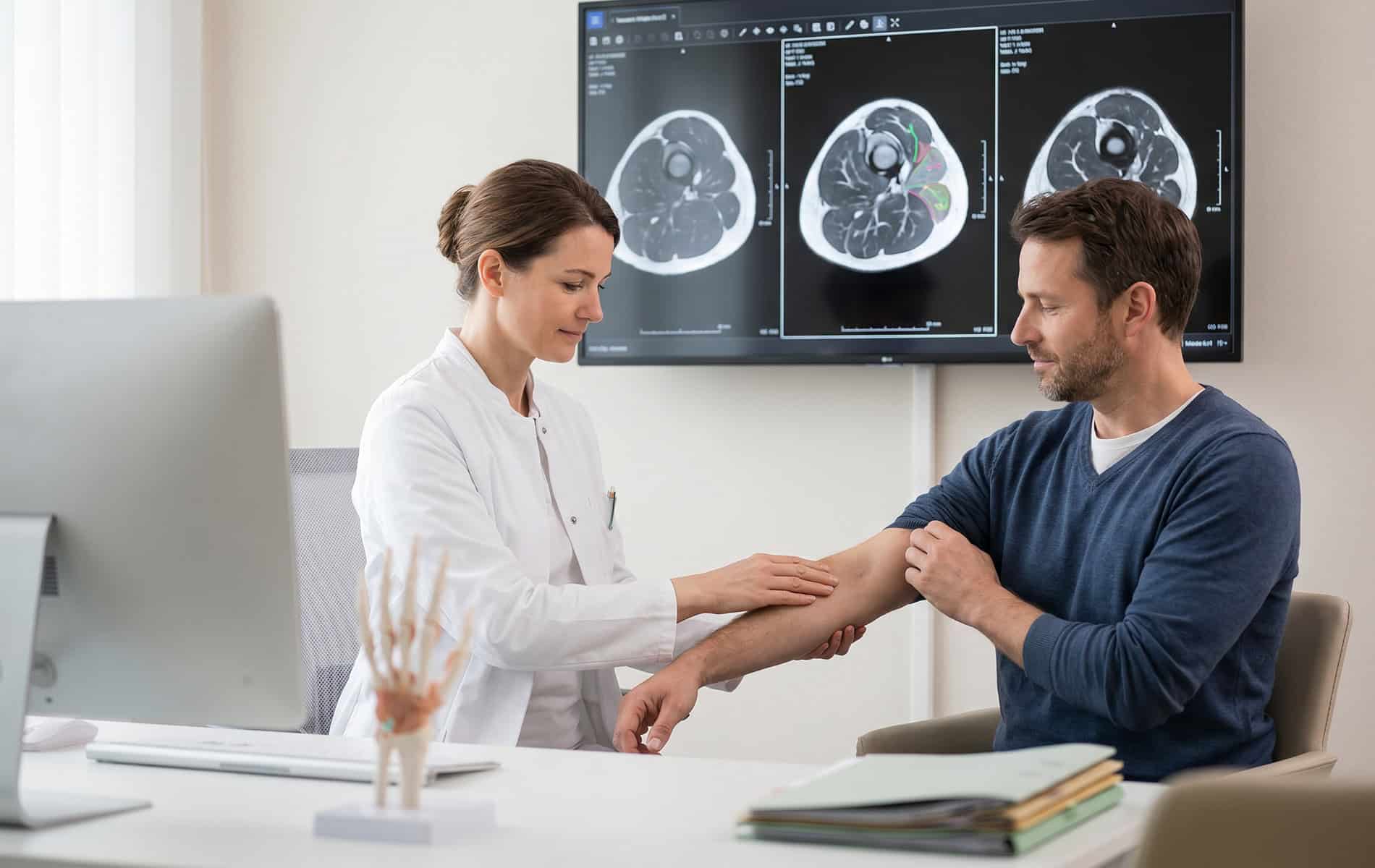
Dieser Effekt erschwert nicht nur die Behandlung, sondern zieht auch das Therapieversagen und die Bildung von Tumorrezidiven nach sich. Deshalb wird in der Medizin nach Methoden zur Früherkennung resistenter Tumorareale gesucht. Verschiedene bildgebende Verfahren (in Kombination mit der Untersuchung bestimmter Tumormarker), die zum Beispiel mit speziellen Tracern arbeiten, erlauben eine Charakterisierung des Tumorgewebes vor und während der Bestrahlung und ermöglichen damit die rechtzeitige Erkennung einer Strahlenresistenz.
Welche Rolle spielt Radioresistenz in der Onkologie?
Wichtige Fakten auf einen Blick:
- Radioresistenz bedeutet die verminderte Empfindlichkeit von Tumorzellen gegenüber ionisierender Strahlung.
- Für die Entstehung der Resistenz kommen verschiedene Ursachen infrage.
- Die Resistenz äußert sich durch eine geringe Tumorregression oder anhaltend hohe Werte der Tumormarker.
Der Begriff „Radioresistenz“ bezieht sich auf die Fähigkeit von Tumorzellen, ionisierende Strahlung so weit zu tolerieren, dass trotz einer in der Regel ausreichenden Strahlendosis nicht die erwarteten Ergebnisse – nämlich die Hemmung des Wachstums und der Untergang der Krebszellen – mit der Strahlentherapie erzielt werden.
Grundsätzlich sind die zu einer Radioresistenz führenden Ursachen vielschichtig und basieren darauf, dass Tumorzellen verschiedene Schutzmechanismen aktivieren können. Signalwege, um den Zelltod (Apoptose) zu verhindern, oder Veränderungen im Stoffwechsel sowie eine höhere Ausschüttung von Schutz- und Reparaturproteinen verringern die Wirksamkeit der durch die Strahlung verursachten Schäden.
Gleichzeitig spielt das Umfeld des Tumors eine Rolle. Bekannt ist, dass Tumore in sauerstoffarmen (hypoxischen) Bereichen die Strahlung besser verkraften und damit Schädigungen der Krebszellen weniger wahrscheinlich werden. Die Radioonkologie muss an dieser Stelle Maßnahmen ergreifen, um entweder die Sättigung in den betreffenden Arealen zu erhöhen (Oxygenierung, unter anderem durch Beatmung in einer Druckkammer) oder die Tumorzellen pharmakologisch so zu beeinflussen, dass sie sensibler auf die ionisierende Strahlung reagieren.
Bei welchen Tumoren ist Radioresistenz besonders verbreitet?
Es gibt eine Reihe von Tumorvarianten (zum Beispiel Lymphome), die meist gut auf die Bestrahlung ansprechen, also eine hohe Strahlenempfindlichkeit aufweisen. Daneben gibt es aber auch Tumore, bei denen eine Radioresistenz eher in Erscheinung tritt:
- Glioblastome sind Hirntumore, bei denen die glioblastomassoziierten Stammzellen (GSC, Glioma Stem Cells) durch verbesserte DNA-Reparaturmechanismen besonders therapieresistent sind.
- In schlecht durchbluteten Tumoren entstehen hypoxische (sauerstoffarme) Regionen, die besonders die Photonenbestrahlung hemmen.
- Bei einigen Weichgewebetumoren (Weichgewebesarkomen) können genetische Variationen zu einer Verringerung der Strahlenempfindlichkeit führen.
Erkennung und Nachweis der Radioresistenz eines Tumors
Wichtige Fakten auf einen Blick:
- Bildgebende Verfahren können resistente Tumorareale identifizieren.
- Funktionelle Aufnahmen ermöglichen die Darstellung der Sauerstoffversorgung.
- Bestimmte Tumormarker liefern Hinweise auf eine potenzielle Strahlenunempfindlichkeit.
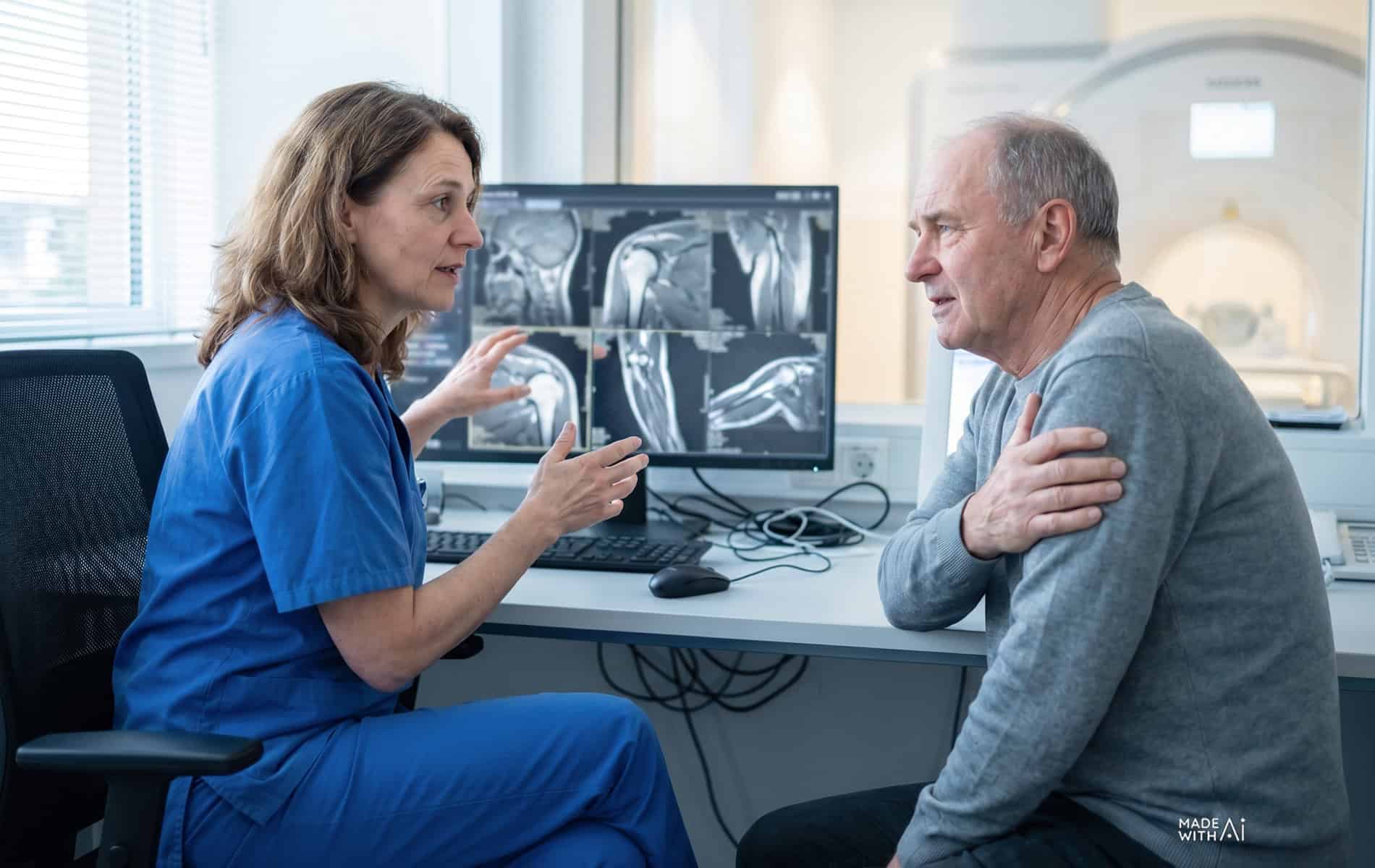
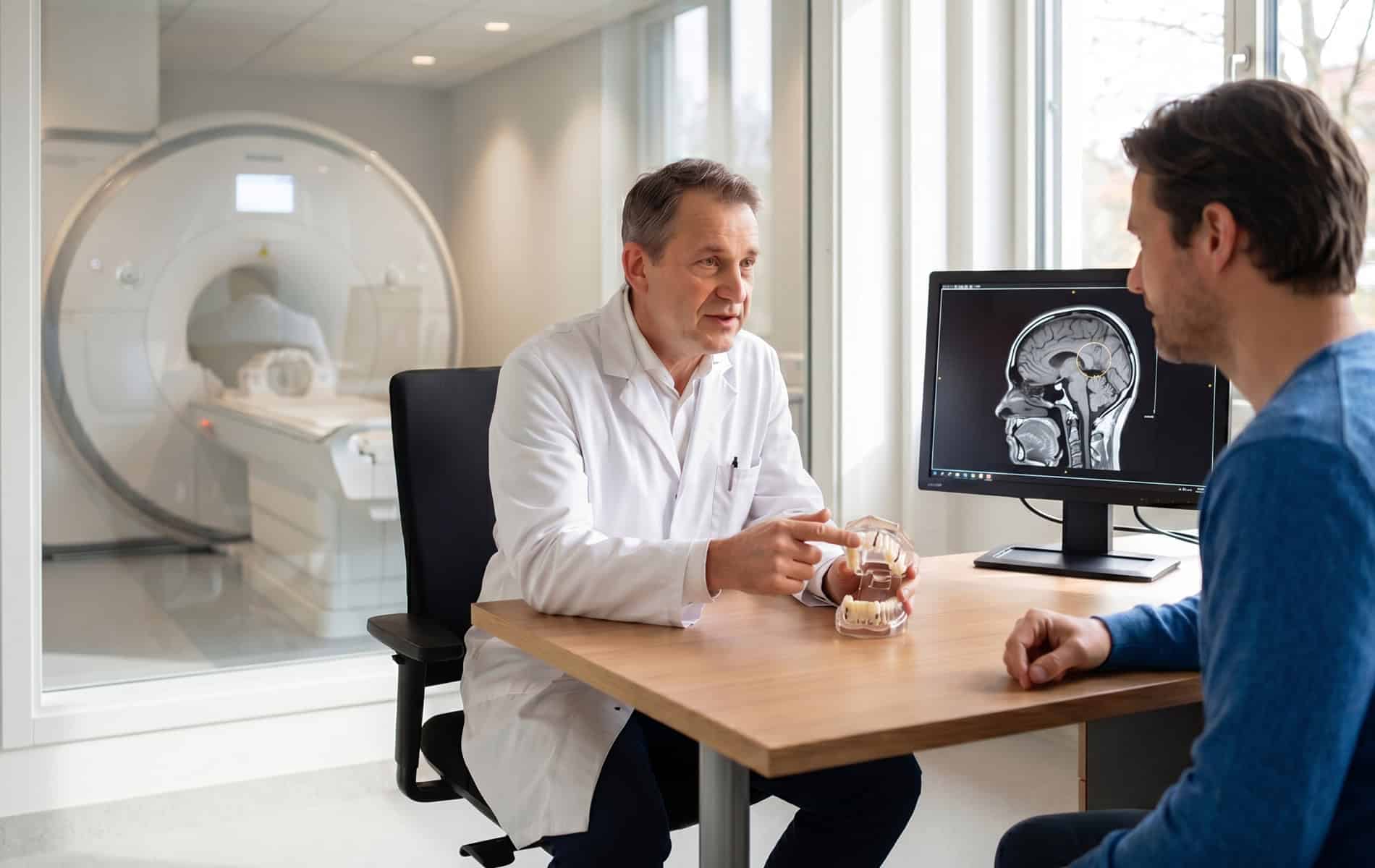
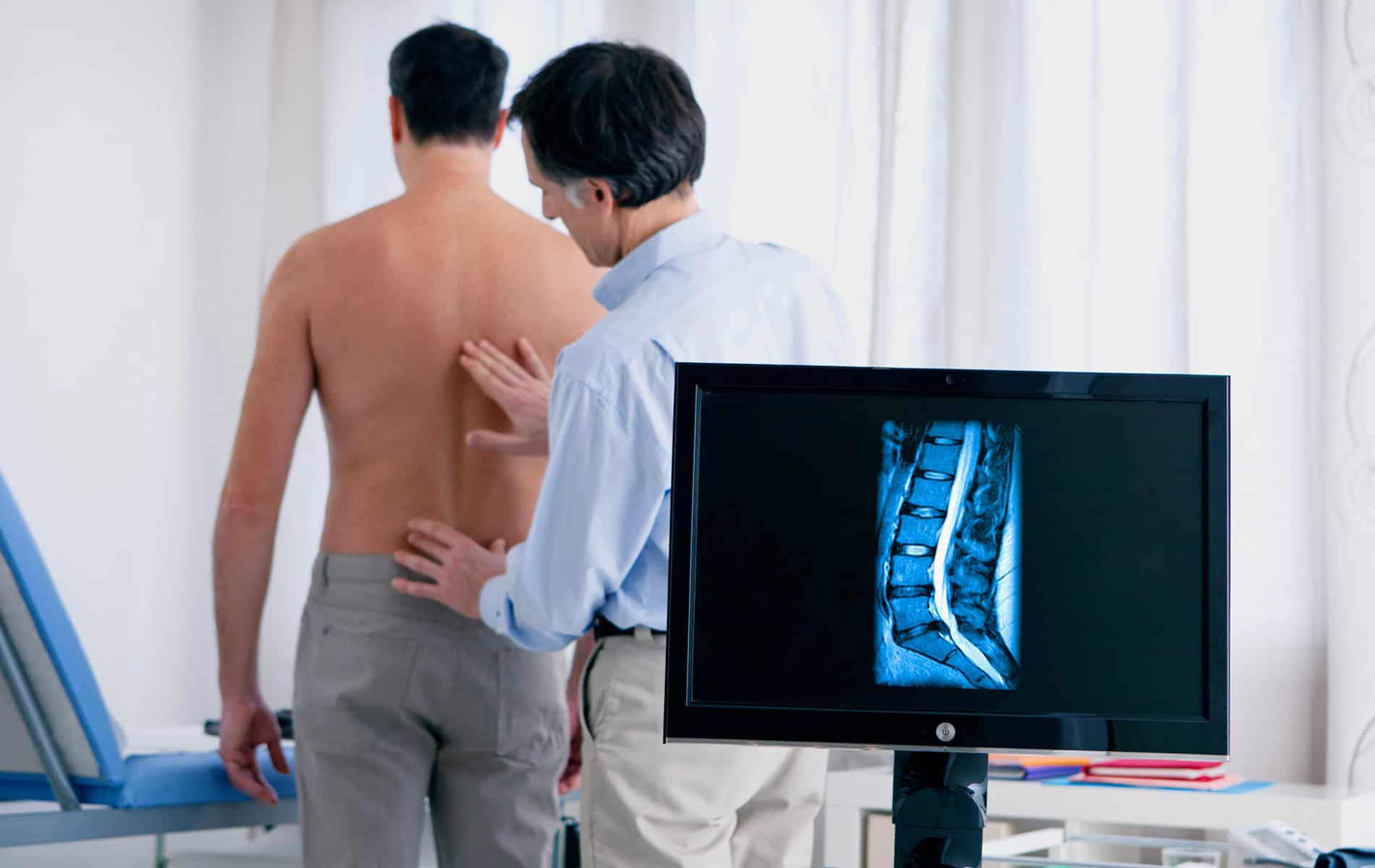
Die Erkennung einer Radioresistenz wirkt sich entscheidend auf den weiteren Therapieverlauf und damit auch auf die Prognose für den individuellen Tumor aus. Idealerweise wird eine Radioresistenz bereits in der Therapieplanung berücksichtigt. Diesbezüglich ist eine genaue Betrachtung der Zielvolumina mittels bildgebender Verfahren, histopathologischer Untersuchungen und molekularer Analysen ein wichtiger Schritt.
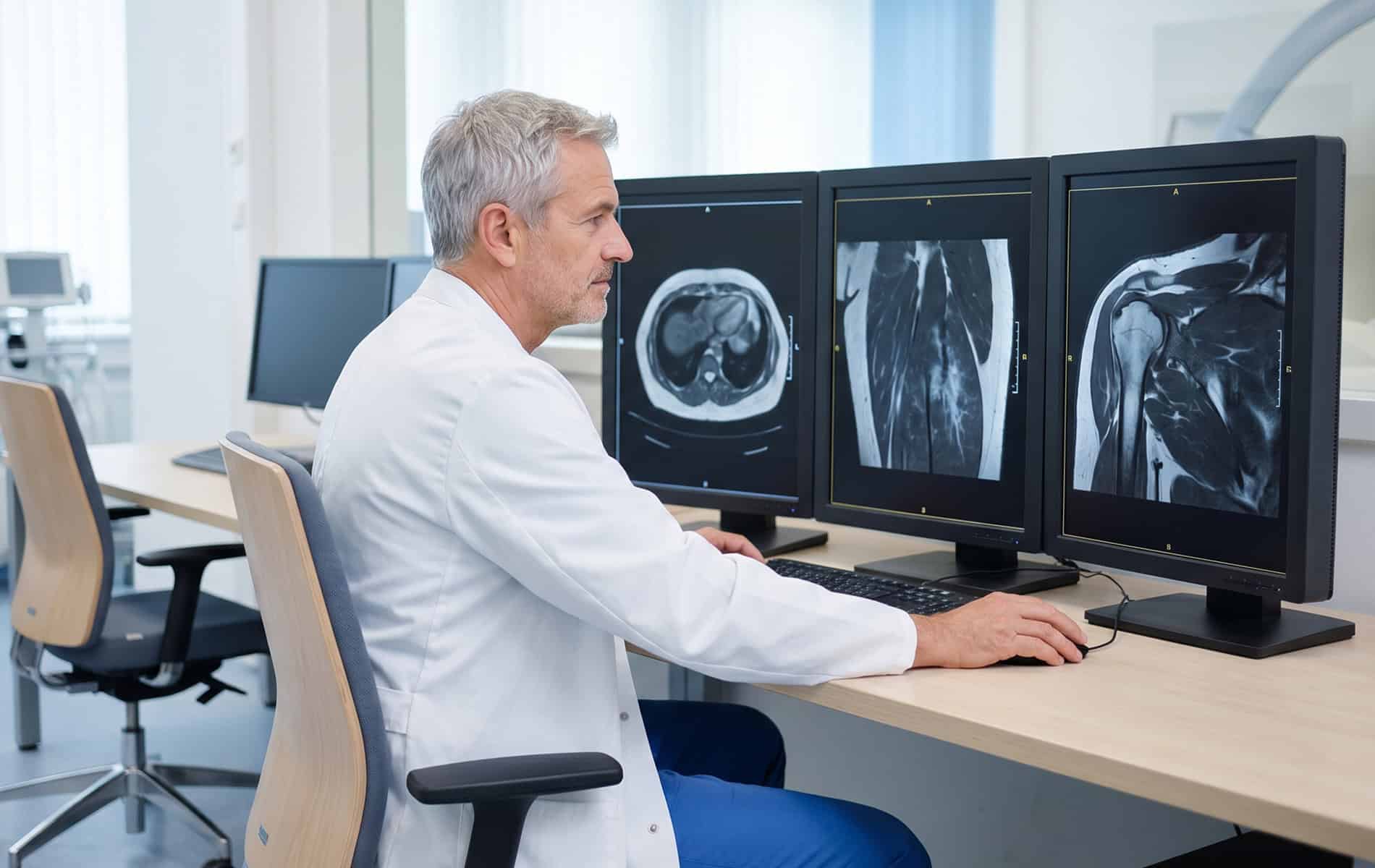
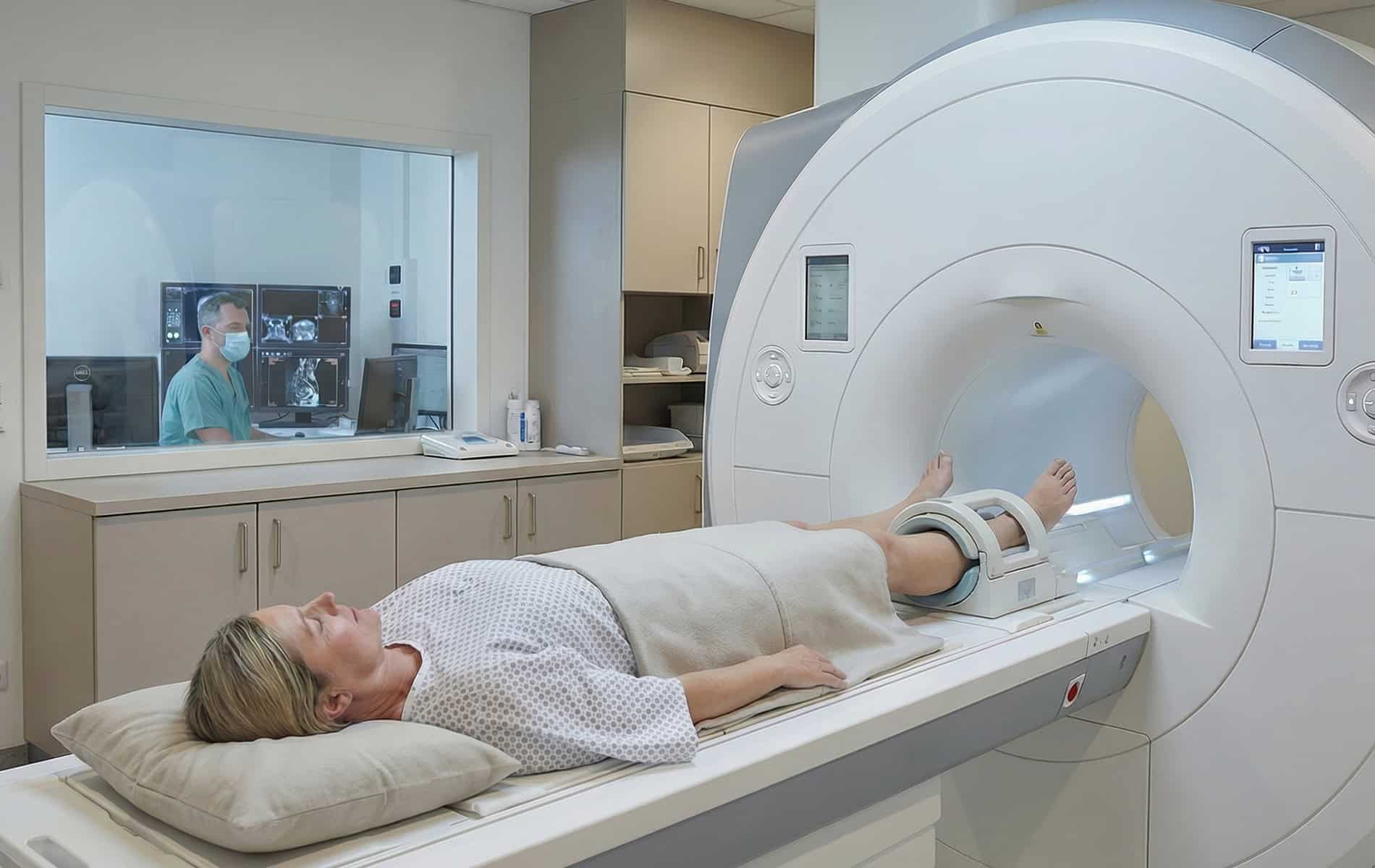
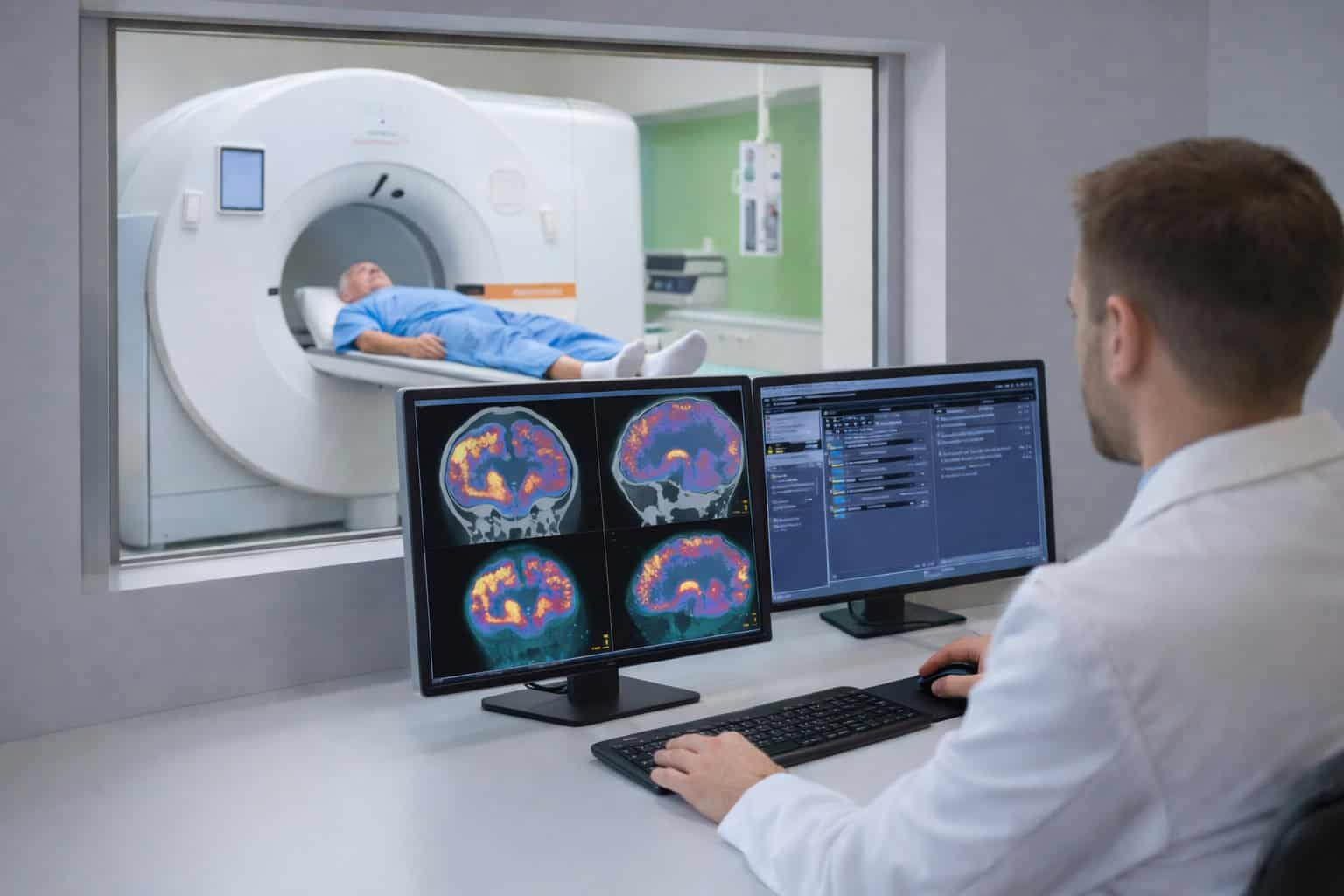
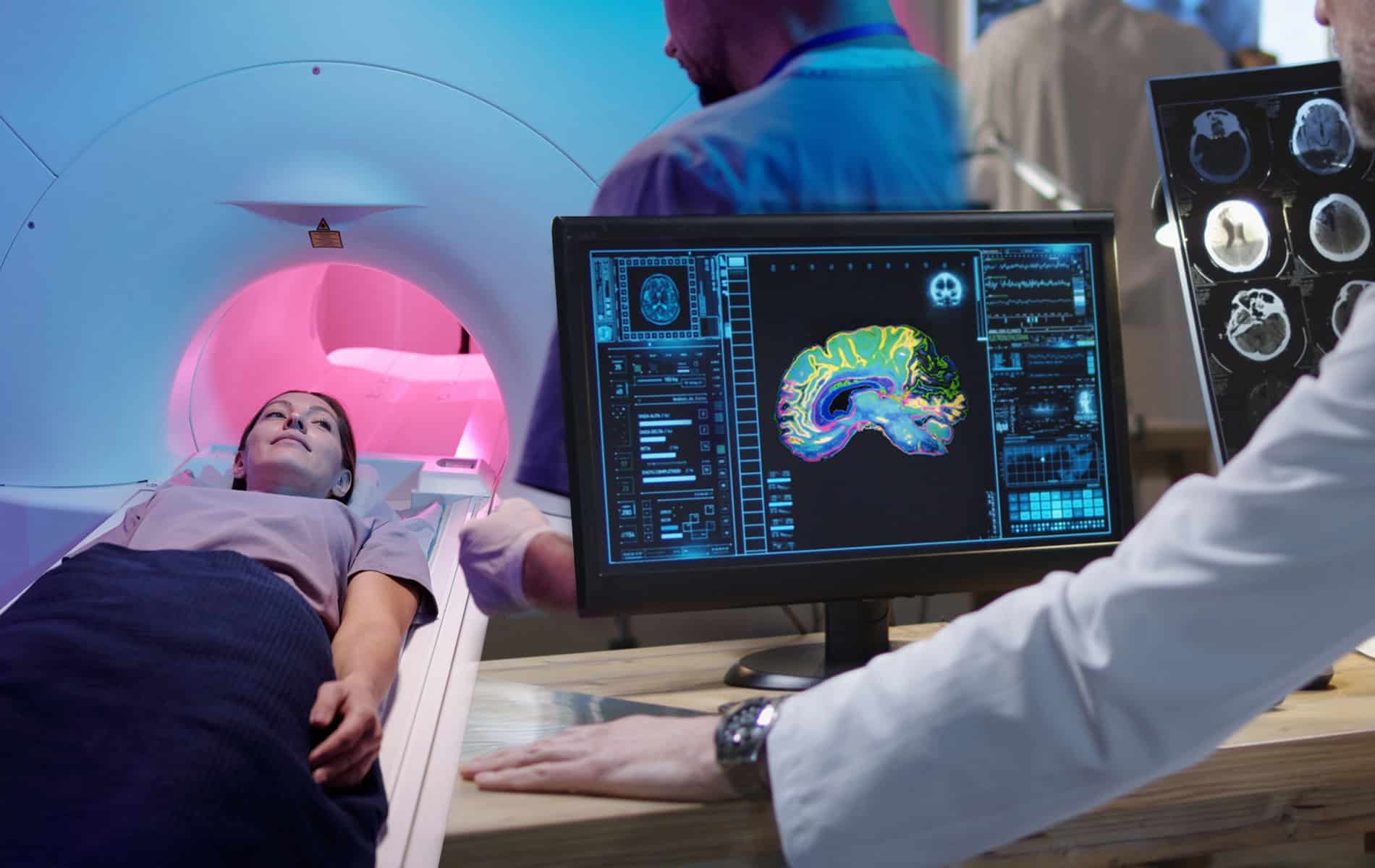
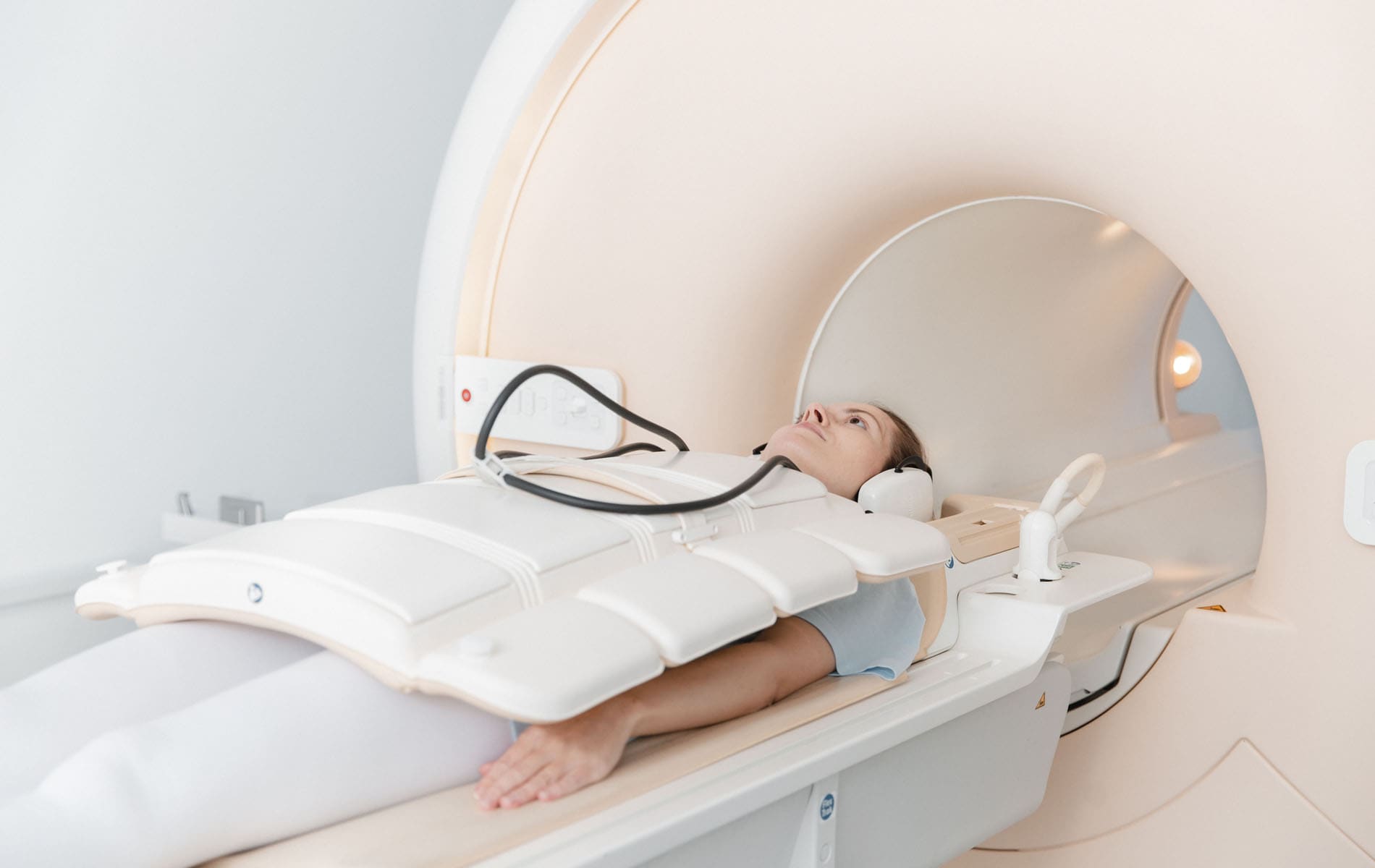
- Mit der Magnetresonanztomographie (MRT) lassen sich in speziellen Sequenzen wie der diffusionsgewichteten Bildgebung (DWI) oder durch besondere Untersuchungsprotokolle (zum Beispiel die Perfusions-MRT) Informationen über die Zelldichte und die Durchblutungsverhältnisse gewinnen. Diese Erkenntnisse erlauben Rückschlüsse auf das Vorliegen hypoxischer Bereiche.
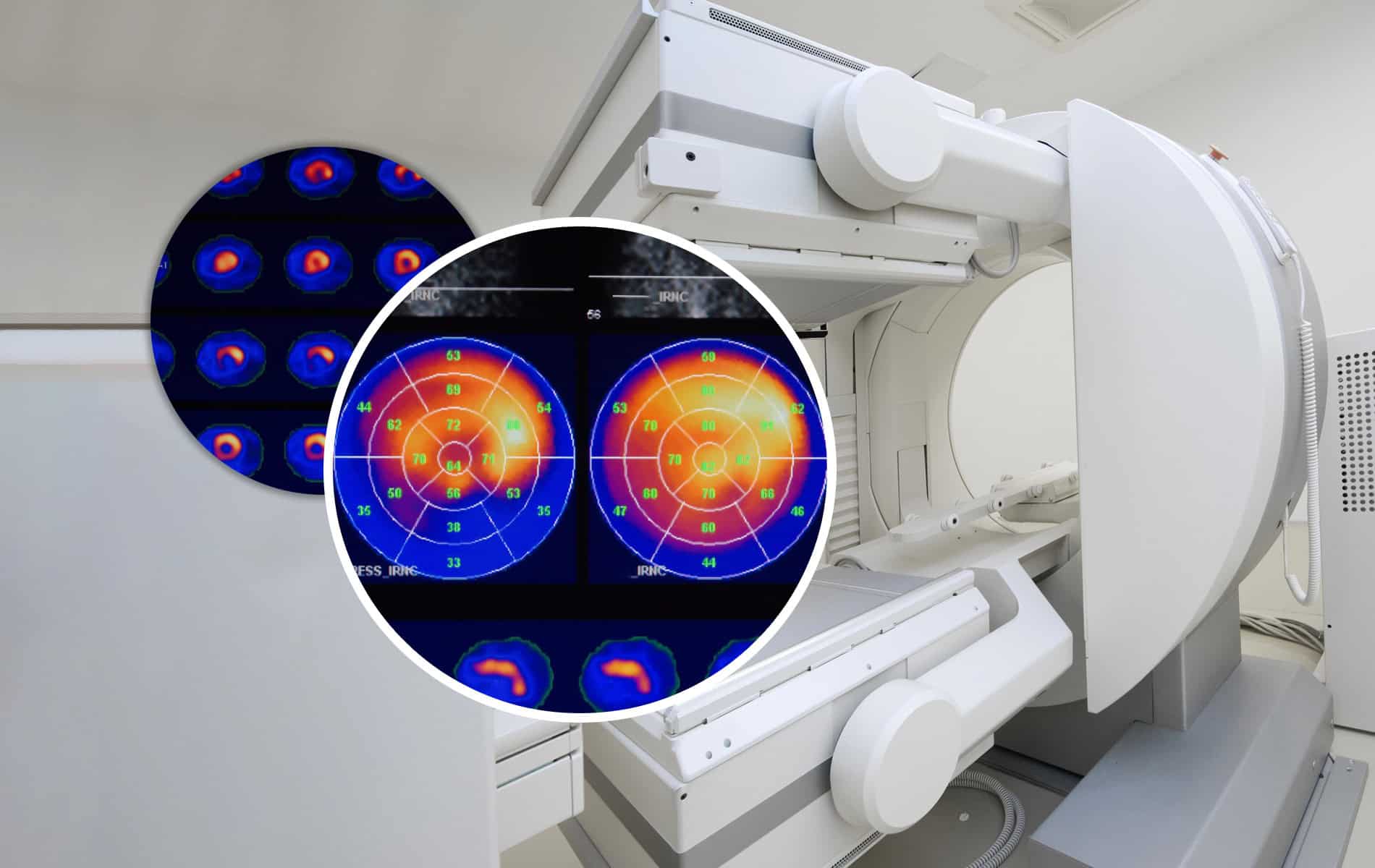
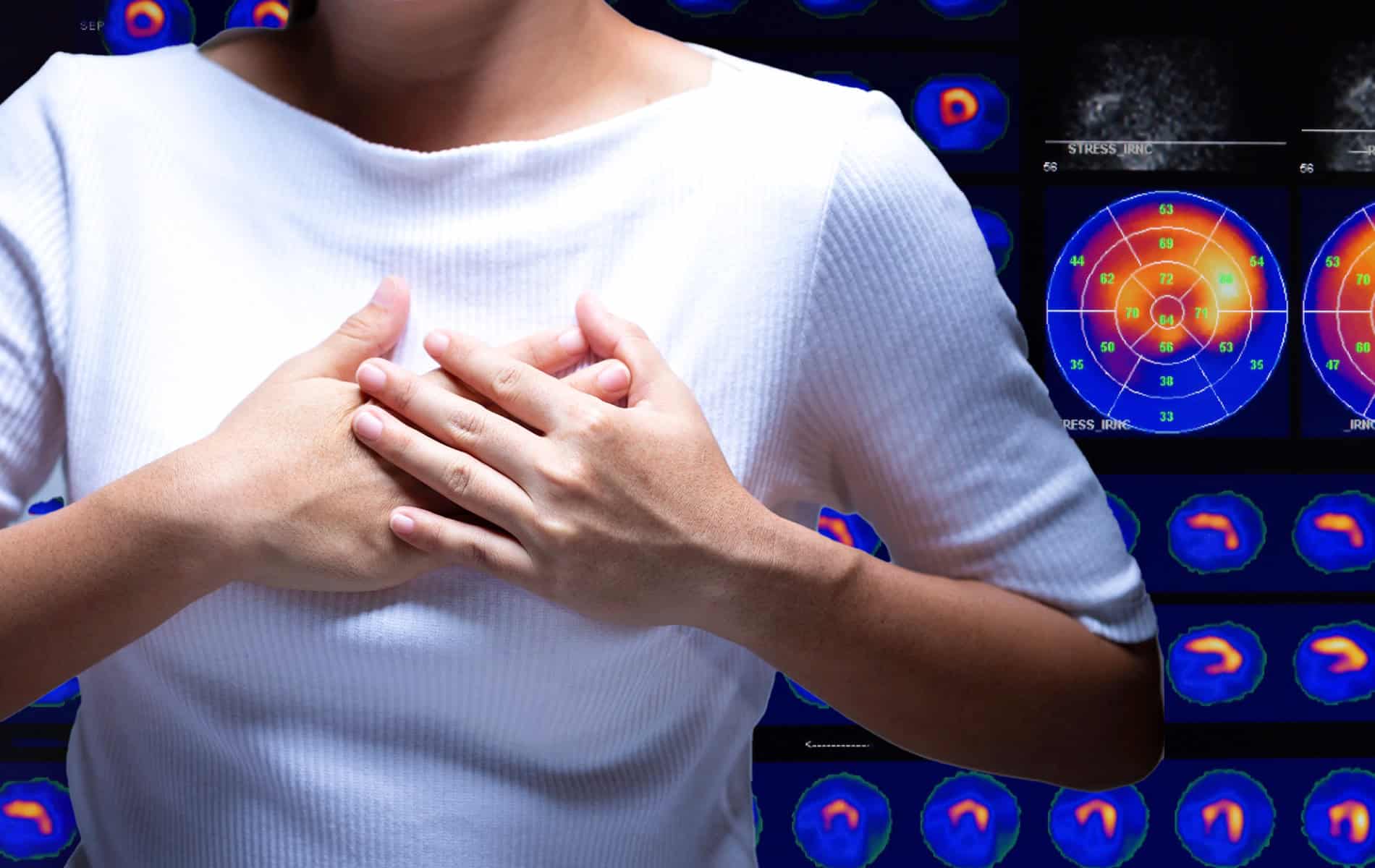
- Mit dem Einsatz hypoxiesensitiver PET-Tracer lassen sich in der Nuklearmedizin nicht nur funktionelle Eigenschaften der Tumore darstellen, sondern auch sauerstoffarme Tumorregionen sichtbar machen, die typischerweise eine erhöhte Strahlenresistenz aufweisen.
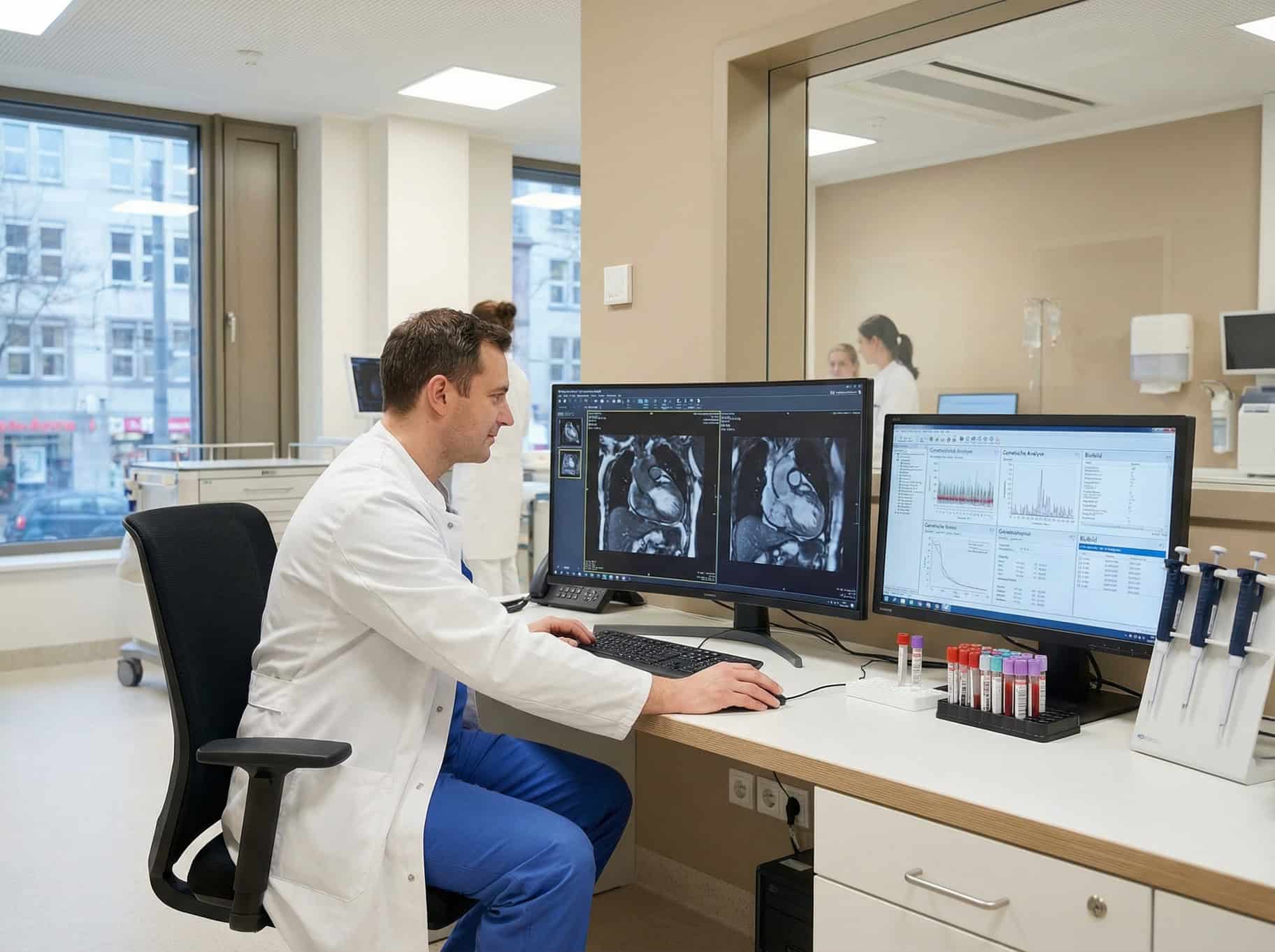
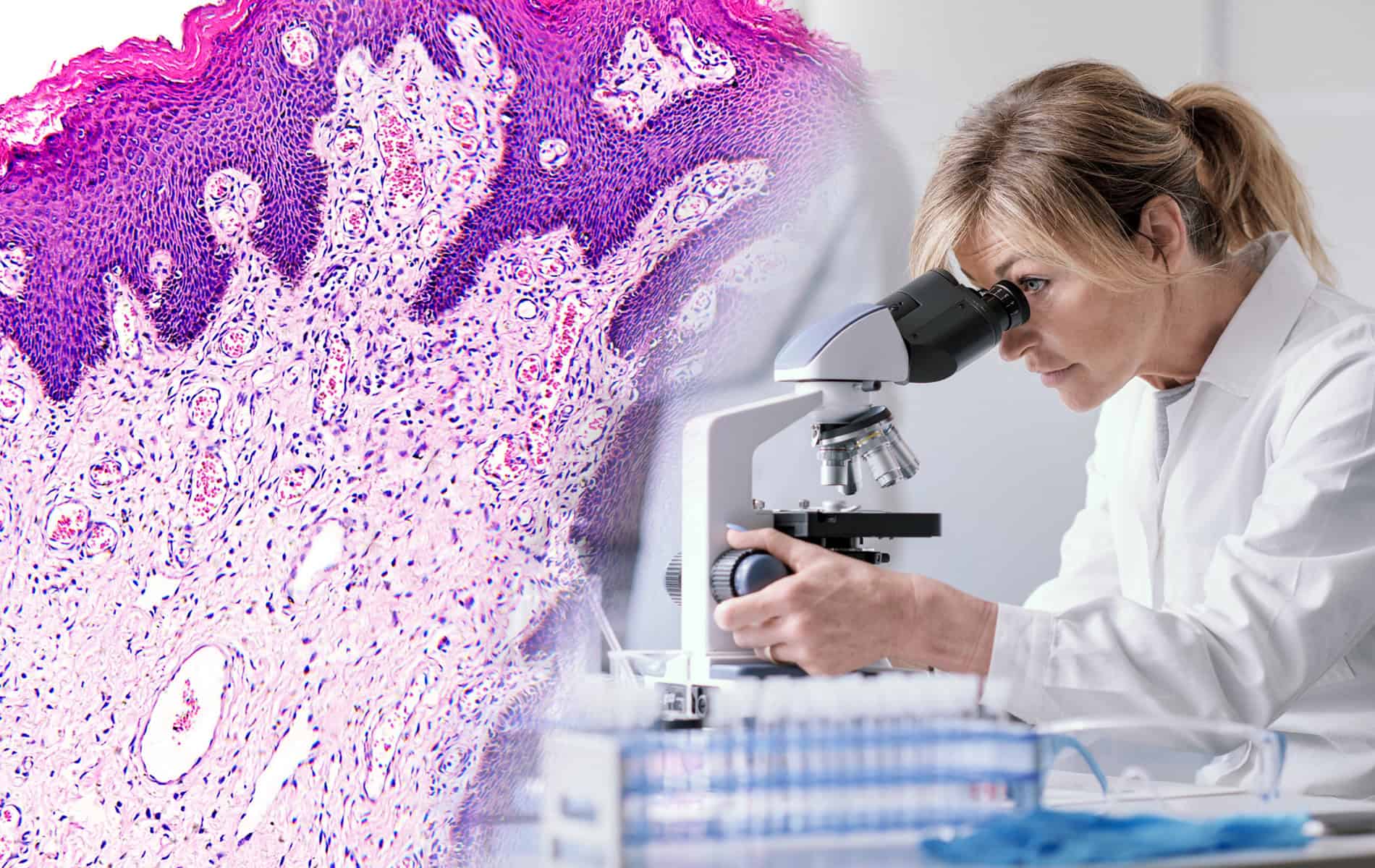
- Mit Untersuchungen auf der zellulären Ebene lässt sich das Vorhandensein von Tumorstammzellen feststellen. Zusätzlich liefert die Molekularpathologie durch die Identifikation spezieller Tumormarker Informationen auf das Vorliegen eines erhöhten Resistenzrisikos.
Strategien zur Überwindung der Radioresistenz
Wichtige Fakten auf einen Blick:
- Bestimmte Medikamente erhöhen die Strahlenempfindlichkeit.
- Eine Kombination von Bestrahlung und Immuntherapie kann das Behandlungsergebnis verbessern.
- Neue Bestrahlungstechniken sind weniger anfällig für hypoxische Szenarien.
In der Radioonkologie stehen inzwischen verschiedene Methoden und Strategien zum Umgang mit Radioresistenzen zur Verfügung. Um ein optimales Handlungsspektrum zu erreichen, gehen verschiedene pharmakologische und technologische Ansätze Hand in Hand. Ziel ist es dabei, Faktoren, welche die Widerstandsfähigkeit der Tumorzellen erhöhen, zu hemmen oder die Strahlendosis im Zielvolumen zu steigern.
Radiosensitizer und Kombinationstherapien
In der Medizin ist es in den letzten Jahren gelungen, verschiedene Radiosensitizer zu identifizieren, mit denen sich die Strahlenempfindlichkeit von Tumorzellen erhöhen lässt. Diese Verbindungen sind in der Lage, spezifische Resistenzmechanismen zu blockieren, um so die Wirksamkeit der Strahlentherapie zu verstärken.
Zum Beispiel hat sich in einer Studie gezeigt, dass der gezielte Einsatz von Wirkstoffen wie Olaparib (PARP-Inhibitor; Poly-ADP-Ribose-Polymerase-Hemmer) die Fähigkeit der Krebszellen zur DNA-Reparatur einschränkt und damit zu einer verbesserten Wirksamkeit der Bestrahlung führt. Besonders ausgeprägt ist diese Eigenschaft bei Tumoren mit bestimmten BRCA1-Mutationen [1].
Einen ähnlichen Ansatz verfolgen Wirkstoffe, wie die ATR-Inhibitoren (Ataxia Telangiectasia and Rad3 Related), die zentrale Reparatur-Signalwege angreifen [2]. Hierdurch werden entscheidende Schutzmechanismen der Tumorzellen blockiert, was eine sensitivere Reaktion auf die einsetzende Bestrahlung bedingt.
Darüber hinaus lassen sich verschiedene Zytostatika, die bereits heute in der Chemotherapie eine zentrale Rolle spielen, in Kombination mit der Strahlentherapie einsetzen. Dahinter steht die Erkenntnis, dass die Substanzen durch Schäden in der Tumor-DNA bzw. die Hemmung der Reparaturzyklen die Sensitivität der Bestrahlung verbessern.
Neben einer Hemmung der Reparaturfähigkeit der Tumore stehen in der Radioonkologie inzwischen auch Ansätze zur Verfügung, mit denen sich die Hypoxie modulieren lässt. Damit kann das Problem der sauerstoffarmen Tumorregionen angegangen und das Behandlungsspektrum für bestimmte Tumore verbessert werden. Mögliche Ansätze bestehen im Einsatz von Vasomodulatoren (Medikamente, mit denen die Durchblutung des Tumors beeinflusst wird) oder Hypoxie-spezifischen Radiosensitizern.
Radioimmuntherapie
In der Krebsbehandlung wird verstärkt versucht, auch die körpereigene Abwehr einzubeziehen. Über spezielle Inhibitoren ist es möglich, das Ansprechen der Immunzellen auf den Tumor zu verbessern. Dabei greifen zwei Aspekte ineinander: Durch die Strahlung werden immunmodulatorische Effekte (abscopaler Effekt) wirksam, die sich gegen den Tumor richten und diesen für die Immunabwehr leichter angreifbar machen. Mithilfe des Einsatzes der Checkpoint-Inhibitoren wird die Tumorumgebung noch stärker geschwächt, was das Ergebnis der Bestrahlung zusätzlich unterstützt.
Protonentherapie und Schwerionentherapie
Beide Varianten gehören zu den physikalischen Ansätzen zur Verhinderung von Radioresistenzen in der Krebsbehandlung. Der Vorteil von Protonentherapie und Schwerionentherapie (eine Methode der Partikeltherapie) besteht darin, dass eine hohe Strahlendosis direkt im Tumor freigesetzt wird, was bei gleichzeitiger Schonung des gesunden Gewebes (Partikelstrahlung gibt beim Gewebeeintritt anfangs wenig Strahlung ab, wodurch die vor dem Tumor liegenden Bereiche geschützt werden) zu einer gezielten Dosiseskalation führt. Ein weiterer Vorteil der Schwerionentherapie (zum Beispiel mit Kohlenstoff) besteht darin, dass diese eine hohe biologische Wirksamkeit aufweist und in Studien bereits zur Behandlung resistenter Tumore zum Einsatz gekommen ist [3]. Zudem sind die neuen Ansätze gegenüber einem hypoxischen Regime weniger empfindlich.
Adaptive Strahlentherapie als Reaktion auf Tumorveränderungen
Sind Veränderungen des Tumors, die zu dessen Resistenz führen, in den Planungsaufnahmen nicht erkennbar, steigt das Risiko für ein Therapieversagen. Mit der Entwicklung adaptiver Bestrahlungskonzepte kann der Bestrahlungsplan während der Behandlung an Veränderungen der Tumorbiologie angepasst werden. Besonders mit der online-adaptiven Radiotherapie (oART oder Online-ART) kann in diesem Zusammenhang sehr schnell reagiert werden, da die Bildaufnahmen hier immer direkt vor den einzelnen Fraktionen (Sitzungen in der Strahlentherapie) stattfinden.
Mehr über LifeLink
Finden Sie jetzt die
Praxis in Ihrer Nähe!
Wir sind überzeugt, dass die Medizin von morgen anders aussehen sollte. Wir sehen den Menschen im Mittelpunkt exzellenter Medizin.
Fazit: Neue Ansätze in der Strahlentherapie können Strahlenresistenz verhindern und die Prognose verbessern
Tumore, die auf eine Bestrahlung nicht wie erhofft reagieren und sich verhältnismäßig resistent zeigen, sind in der Radioonkologie eine Herausforderung. Mittlerweile stehen der Medizin diesbezüglich jedoch verschiedene Lösungsansätze zur Verfügung. Diese umfassen sowohl die verstärkte Sensibilisierung der Tumore gegenüber ionisierender Strahlung als auch den Einsatz neuer Protokolle, die Verwendung von künstlicher Intelligenz und die Nutzung von Strahlung, mit der eine biologisch wirksame Dosis direkt im Tumor freigesetzt wird. Auf diese Weise kann auf eine Radioresistenz in vielen Fällen angemessen reagiert werden.
FAQ zu den Ansätzen zur Überwindung der Radioresistenz: Die wichtigsten Fragen und Antworten
Ist ein radioresistenter Tumor schon in der Diagnostik zu erkennen?
Da Strahlungsresistenz bei Krebs verschiedene Ursachen haben kann und ein komplexes Zusammenspiel verschiedener Mechanismen ist, lässt sich die Wahrscheinlichkeit ihres Eintretens nicht ohne Weiteres abschätzen. Im Rahmen bildgebender Verfahren, mit denen die Durchblutung des Tumors darstellbar ist, lassen sich hypoxische Areale identifizieren. Marker für die Reparaturfähigkeit oder bestimmte Tumorstammzellen sind nur mit der Molekularpathologie oder Histologie nachweisbar.
Wie zeigt sich ein radioresistenter Tumor unter der Bestrahlung?
Die Anzeichen für einen radioresistenten Tumor sind sehr unterschiedlich. In der Bildgebung, wie einem MRT oder der Computertomographie (CT) ist eine unzureichende Tumorregression (Verringerung des Volumens bzw. der Tumormasse) zu beobachten. Gleichzeitig verändern sich die Werte für die verschiedenen Tumormarker nicht wie erhofft, beispielsweise kann bei einem Prostatakarzinom der PSA-Wert weiterhin sehr hoch sein. Allerdings muss gerade bei den strukturellen Veränderungen eine genaue Bewertung der Situation stattfinden. Dies betrifft unter anderem die Frage, ob kritische Strukturen eventuell Narbengewebe oder andere strahleninduzierte Läsionen darstellen können.
Wie wird auf Radioresistenz während der Bestrahlung reagiert?
In der Radioonkologie gibt es mehrere Möglichkeiten, um auf eine während der Therapie erkannte Radioresistenz zu reagieren. zum Beispiel mit der oART oder einer Kombinationstherapie (die auf Radiosensitizer setzt). Allerdings stoßen die Reaktionsmöglichkeiten auf Grenzen, da sich nicht jede Resistenz während der Therapie sofort überwinden lässt und der behandelnde Arzt immer die Belastung durch Nebenwirkungen als limitierenden Faktor im Auge behalten muss.
[1] Bi Y, Verginadis II, Dey S, Lin L, Guo L, Zheng Y, Koumenis C. Radiosensitization by the PARP inhibitor olaparib in BRCA1-proficient and deficient high-grade serous ovarian carcinomas. Gynecol Oncol. 2018 Sep;150(3):534-544. doi: 10.1016/j.ygyno.2018.07.002. Epub 2018 Jul 17. PMID: 30025822.
[2] Sharma R, Mishra A, Bhardwaj M, Singh G, Indira Harahap LV, Vanjani S, Pan CH, Nepali K. Medicinal chemistry breakthroughs on ATM, ATR, and DNA-PK inhibitors as prospective cancer therapeutics. J Enzyme Inhib Med Chem. 2025 Dec;40(1):2489720. doi: 10.1080/14756366.2025.2489720. Epub 2025 Apr 21. PMID: 40256842; PMCID: PMC12013171.
[3] Pompos A, Durante M, Choy H. Heavy Ions in Cancer Therapy. JAMA Oncol. 2016 Dec 1;2(12):1539-1540. doi: 10.1001/jamaoncol.2016.2646. PMID: 27541302; PMCID: PMC5894097.